Iklan
Pertanyaan
Data eksperimen untuk reaksi : 2 A ( g ) + B 2 ( g ) → 2 AB ( g ) Tentukan: a. orde reaksi total b. persamaanlaju reaksi c. nilai konstanta (k) d. tentukan laju reaksi jika konsentrasi gas A = 2 dan B = 4
Data eksperimen untuk reaksi :
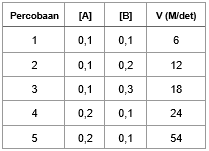
Tentukan:
a. orde reaksi total
b. persamaan laju reaksi
c. nilai konstanta (k)
d. tentukan laju reaksi jika konsentrasi gas A = 2 dan B = 4
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
10
5.0 (7 rating)
zM
zaki Mulyadi syahputra
Makasih ❤️
AP
Andini Putri
Penjelasannya mudah dipahami❤️ Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















