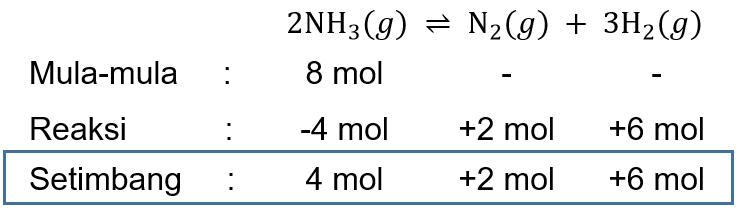Iklan
Pertanyaan
Dalam wadah 3 liter, 8 mol amonia terurai dengan derajat disosiasi 0,5 menurut reaksi berikut : 2 NH 3 ( g ) ⇌ N 2 ( g ) + 3 H 2 ( g ) Tekanan pada kesetimbangan adalah 3,5 atm. Besar tetapan kesetimbangan ( K p ) adalah ....
Dalam wadah 3 liter, 8 mol amonia terurai dengan derajat disosiasi 0,5 menurut reaksi berikut :
Tekanan pada kesetimbangan adalah 3,5 atm. Besar tetapan kesetimbangan () adalah ....
Iklan
DE
D. Entry
Master Teacher
Jawaban terverifikasi
20
5.0 (6 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia