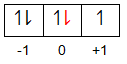Iklan
Pertanyaan
Bilangan kuantum dari elektron terakhirsuatu unsur, yaitu n = 3 , ℓ = 1 , m = 0 , s = − 2 1 . Nomor atom unsur tersebut adalah ....
Bilangan kuantum dari elektron terakhir suatu unsur, yaitu . Nomor atom unsur tersebut adalah ....
17
21
25
28
30
Iklan
FT
F. Tri
Master Teacher
Jawaban terverifikasi
2
4.2 (5 rating)
Iklan
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia