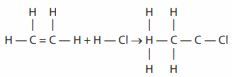Iklan
Pertanyaan
Besarnya perubahan entalpi pada reaksi : CH 2 = CH 2 + HCl → CH 3 − CH 2 Cl Jika diketahui energi rata-rata : C = C = 614 mol kJ C − C = 348 mol kJ C − H = 413 mol kJ C − Cl = 328 mol kJ H − Cl = 431 mol kJ
Besarnya perubahan entalpi pada reaksi :
Jika diketahui energi rata-rata :
-175 kJ.
-44 kJ.
+44 kJ.
+175 kJ.
+475 kJ.
Iklan
Q'
Q. 'Ainillana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
2
2.8 (5 rating)
ZA
Zahrina Aulia
Pembahasan tidak lengkap
cr
cut riva
Pembahasan tidak lengkap
H
Hilda
Pembahasan tidak menjawab soal Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia