Iklan
Pertanyaan
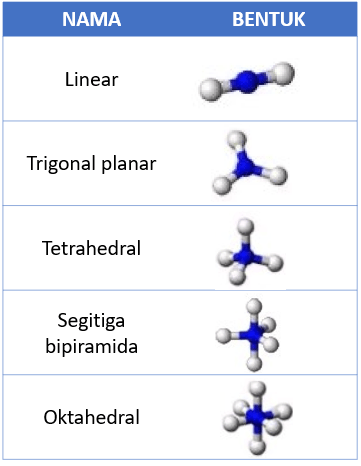
Berdasarkan pernyataan bentuk molekul di bawah ini merupakan pernyataan dari teori….
Berdasarkan pernyataan bentuk molekul di bawah ini merupakan pernyataan dari teori….
Teori hibridisasi
Teori domain elektron
Aturan oktet
Aturan duplet
Struktur lewis
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
3
5.0 (2 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia