Iklan
Pertanyaan
Bacalah bacaan berikut! Kepolaran Senyawa Kovalen Ikatan kovalen terbentuk karena pemakaian pasangan elektron bersama, dimana masing - masing atom yang berikatan menyumbangkan sebuah elektron dan membentuk sepasang elektron untuk dipakai bersama. Apabila pasangan elektron hanya berasal dari salah satu atom yang berikatan, maka ikatan yang terbentuk disebut Ikatan Kovalen Koordinasi. Elektron tidak selalu dibagi rata antara dua atom yang berikatan. Satu atom mungkin lebih kuat untuk menarik elektron ke dirinya sendiri dibanding dengan atom lain. Tarikan ini disebut sebagai elektronegativitas. Pembagian elektron yang tidak merata dalam ikatan mengakibatkan pembentukan dipol listrik (kepolaran), yaitu pemisahan muatan listrik positif dan negatif. Penentuan polaritas ikatan kovalen dapat menggunakan cara numerik, yaitu menghitung perbedaan elektronegativitas atom yang saling berikatan. Senyawa polar adalah senyawa yang mempunyai momen dipol lebih dari nol sedangkan senyawa nonpolar momen dipolnya sama dengan nol Selain dilihat dari momen dipol, kepolaran suatu senyawa dapat dilihat dari bentuk molekul. Bentuk molekul simetris merupakan senyawa nonpolar, sedangkan bentuk molekul asimetris merupakan senyawa polar. Perbedeaan kepolaran senyawa kovalen akan menentukan sifat fisiknya, seperti wujud pada suhu kamar, kelarutan dalam air, dan konduktivitas larutan dalam listrik. Perhatikan data hasil pengamatan uji seyawa kovalen polar dan nonpolar berikut!
Bacalah bacaan berikut!
Kepolaran Senyawa Kovalen
Ikatan kovalen terbentuk karena pemakaian pasangan elektron bersama, dimana masing - masing atom yang berikatan menyumbangkan sebuah elektron dan membentuk sepasang elektron untuk dipakai bersama. Apabila pasangan elektron hanya berasal dari salah satu atom yang berikatan, maka ikatan yang terbentuk disebut Ikatan Kovalen Koordinasi.
Elektron tidak selalu dibagi rata antara dua atom yang berikatan. Satu atom mungkin lebih kuat untuk menarik elektron ke dirinya sendiri dibanding dengan atom lain. Tarikan ini disebut sebagai elektronegativitas. Pembagian elektron yang tidak merata dalam ikatan mengakibatkan pembentukan dipol listrik (kepolaran), yaitu pemisahan muatan listrik positif dan negatif.
Penentuan polaritas ikatan kovalen dapat menggunakan cara numerik, yaitu menghitung perbedaan elektronegativitas atom yang saling berikatan. Senyawa polar adalah senyawa yang mempunyai momen dipol lebih dari nol sedangkan senyawa nonpolar momen dipolnya sama dengan nol Selain dilihat dari momen dipol, kepolaran suatu senyawa dapat dilihat dari bentuk molekul. Bentuk molekul simetris merupakan senyawa nonpolar, sedangkan bentuk molekul asimetris merupakan senyawa polar. Perbedeaan kepolaran senyawa kovalen akan menentukan sifat fisiknya, seperti wujud pada suhu kamar, kelarutan dalam air, dan konduktivitas larutan dalam listrik. Perhatikan data hasil pengamatan uji seyawa kovalen polar dan nonpolar berikut!
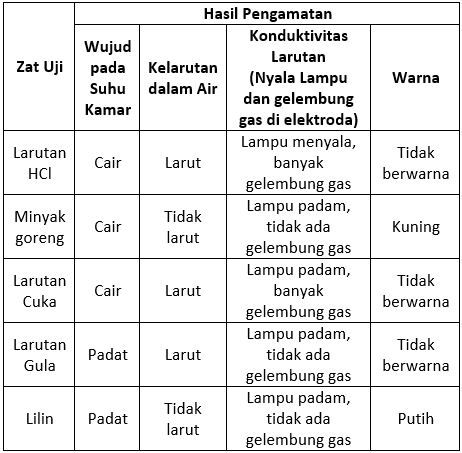
Gula dapat larut dalam minyak goreng sebagaimana gula larut dalam air.
murni dan larutannya dapat menghantarkan listrik.
Larutan cuka tidak dapat larut dalam minyak goreng.
Senyawa kovalen polar pada suhu ruangan hanya didapatkan dalam wujud padat dan tidak berwarna.
Iklan
I. Solichah
Master Teacher
19
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















