Sry E
01 Juni 2025 07:59
Iklan
Sry E
01 Juni 2025 07:59
Pertanyaan
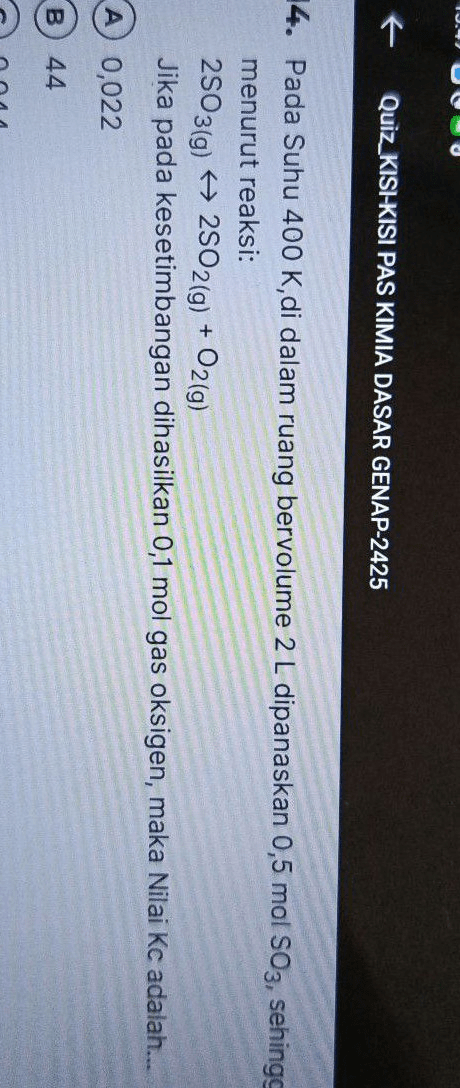
Pada suhu 400k, di dalam ruang bervolume 2 L dipanaskan mol SO3, sehingga terurai menurut reaksi : 2SO3 (g)<—> 2SO2(g) +O2(g) Jika pada kesetimbangan dihasilkan 0,1 mol gas oksigen maka nilai KC adalah A. 0,022 B. 44 C.0, 044 D. 2,2
Pada suhu 400k, di dalam ruang bervolume 2 L dipanaskan mol SO3, sehingga terurai menurut reaksi :
2SO3 (g)<—> 2SO2(g) +O2(g)
Jika pada kesetimbangan dihasilkan 0,1 mol gas oksigen maka nilai KC adalah
A. 0,022
B. 44
C.0, 044
D. 2,2
9
1
Iklan
Rion K
01 Juni 2025 08:34
<p>Kita asumsikan pada awalnya hanya ada SO₃ dan jumlah mol SO₃ = 0,5 mol. Reaksi yang terjadi adalah:</p><p>2 SO₃ (g) ⟷ 2 SO₂ (g) + O₂ (g)</p><p>Misalkan perubahan reaksi (ekstensitas) dinyatakan dengan x. Sesuai stoikiometri reaksi, perubahan tiap zat adalah:</p><ul><li>SO₃ berkurang 2x</li><li>SO₂ bertambah 2x</li><li>O₂ bertambah x</li></ul><p>Diketahui bahwa pada kesetimbangan jumlah mol O₂ = 0,1, sehingga: x = 0,1</p><p>Maka, pada kesetimbangan: • Mol SO₃ = 0,5 - 2 x 0,1 = 0,5 - 0,2 = 0,3 mol<br>• Mol SO₂ = 2 x 0,1 = 0,2 mol<br>• Mol O₂ = 0,1 mol</p><p>Karena volume ruang adalah 2 L, konsentrasi masing-masing zat adalah: • [SO₃] = 0,3 : 2 = 0,15 M<br>• [SO₂] = 0,2 : 2 = 0,1 M<br>• [O₂] = 0,1 : 2 = 0,05 M</p><p>Rumus tetapan kesetimbangan konsentrasi (K₍C₎) untuk reaksi ini adalah:</p><p>K₍C₎ = ([SO₂]² x [O₂]) : ([SO₃]²)</p><p>Substitusi nilai-nilai: K₍C₎ = ((0,1)² x 0,05) : ((0,15)²)</p><p>Hitung langkah demi langkah:</p><ol><li>(0,1)² = 0,01</li><li>(0,15)² = 0,0225</li><li>0,01 x 0,05 = 0,0005</li><li>0,0005 : 0,0225 ≈ 0,022</li></ol><p>Jadi, nilai K₍C₎ adalah <strong>0,022</strong>.</p>
Kita asumsikan pada awalnya hanya ada SO₃ dan jumlah mol SO₃ = 0,5 mol. Reaksi yang terjadi adalah:
2 SO₃ (g) ⟷ 2 SO₂ (g) + O₂ (g)
Misalkan perubahan reaksi (ekstensitas) dinyatakan dengan x. Sesuai stoikiometri reaksi, perubahan tiap zat adalah:
- SO₃ berkurang 2x
- SO₂ bertambah 2x
- O₂ bertambah x
Diketahui bahwa pada kesetimbangan jumlah mol O₂ = 0,1, sehingga: x = 0,1
Maka, pada kesetimbangan: • Mol SO₃ = 0,5 - 2 x 0,1 = 0,5 - 0,2 = 0,3 mol
• Mol SO₂ = 2 x 0,1 = 0,2 mol
• Mol O₂ = 0,1 mol
Karena volume ruang adalah 2 L, konsentrasi masing-masing zat adalah: • [SO₃] = 0,3 : 2 = 0,15 M
• [SO₂] = 0,2 : 2 = 0,1 M
• [O₂] = 0,1 : 2 = 0,05 M
Rumus tetapan kesetimbangan konsentrasi (K₍C₎) untuk reaksi ini adalah:
K₍C₎ = ([SO₂]² x [O₂]) : ([SO₃]²)
Substitusi nilai-nilai: K₍C₎ = ((0,1)² x 0,05) : ((0,15)²)
Hitung langkah demi langkah:
- (0,1)² = 0,01
- (0,15)² = 0,0225
- 0,01 x 0,05 = 0,0005
- 0,0005 : 0,0225 ≈ 0,022
Jadi, nilai K₍C₎ adalah 0,022.
· 5.0 (1)
Iklan
Mau jawaban yang terverifikasi?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



