ST
Salsabilla T
29 Juli 2024 13:52
Iklan
ST
Salsabilla T
29 Juli 2024 13:52
Pertanyaan
Mohon di bantu jawab
Mohon di bantu jawab

1
1
Iklan
YD
Yarta D
29 Juli 2024 21:57
Jawaban terverifikasi
<p>Aturan penentuan bilangan oksidasi</p><ol><li><strong>Biloks unsur bebas = 0 </strong>(Unsur bebas adalah unsur yang berdiri sendiri atau berikatan dengan sesama atomnya, contohnya Na, Cr, Ni, O<sub>2</sub>, H<sub>2</sub>, dsb)</li><li><strong>Biloks golongan IA = +1 dan golongan IIA = +2</strong></li><li><strong>Jumlah biloks unsur-unsur pembentuk senyawa = 0 </strong>(contohnya : NaCl = biloks Na + biloks Cl = 0)</li><li><strong>Biloks atom-atom penyusun dalam ion sama dengan muatannya</strong> (contohnya = biloks Cl<sup>- </sup>= -1)</li><li><strong>Biloks unsur fluorin (F) dalam senyawa selalu = -1</strong></li><li><strong>Biloks unsur Hidrogen (H) dalam senyawa = +1</strong>, kecuali pada senyawa hibrida (senyawa hibrida yaitu senyawa yang terbentuk dari unsur logam dengan atom hidrogen, contohnya NaH)</li><li><strong>Biloks unsur Oksigen (O) dalam senyawa = -2</strong>, kecuali senyawa peroksida(H<sub>2</sub>O<sub>2</sub>), superoksida(NaO<sub>2</sub>), dan oksifluorida(OF<sub>2</sub>)</li></ol><p> </p><p>Pengertian reaksi redoks berdasarkan bilangan biloks</p><ul><li><strong>Reaksi Reduksi</strong> : zat yang mengalami penurunan bilangan oksidasi </li><li><strong>Reaksi Oksidasi</strong> : zat yang mengalami kenaikan bilangan oksidasi </li></ul><p> </p><p>Pengertian reduktor dan oksidator</p><ul><li><strong>Reduktor</strong> : zat yang mereduksi atau yang mengalami oksidasi </li><li><strong>Oksidator</strong> : zat yang mengoksidasi atau yang mengalami reduksi</li></ul>
Aturan penentuan bilangan oksidasi
- Biloks unsur bebas = 0 (Unsur bebas adalah unsur yang berdiri sendiri atau berikatan dengan sesama atomnya, contohnya Na, Cr, Ni, O2, H2, dsb)
- Biloks golongan IA = +1 dan golongan IIA = +2
- Jumlah biloks unsur-unsur pembentuk senyawa = 0 (contohnya : NaCl = biloks Na + biloks Cl = 0)
- Biloks atom-atom penyusun dalam ion sama dengan muatannya (contohnya = biloks Cl- = -1)
- Biloks unsur fluorin (F) dalam senyawa selalu = -1
- Biloks unsur Hidrogen (H) dalam senyawa = +1, kecuali pada senyawa hibrida (senyawa hibrida yaitu senyawa yang terbentuk dari unsur logam dengan atom hidrogen, contohnya NaH)
- Biloks unsur Oksigen (O) dalam senyawa = -2, kecuali senyawa peroksida(H2O2), superoksida(NaO2), dan oksifluorida(OF2)
Pengertian reaksi redoks berdasarkan bilangan biloks
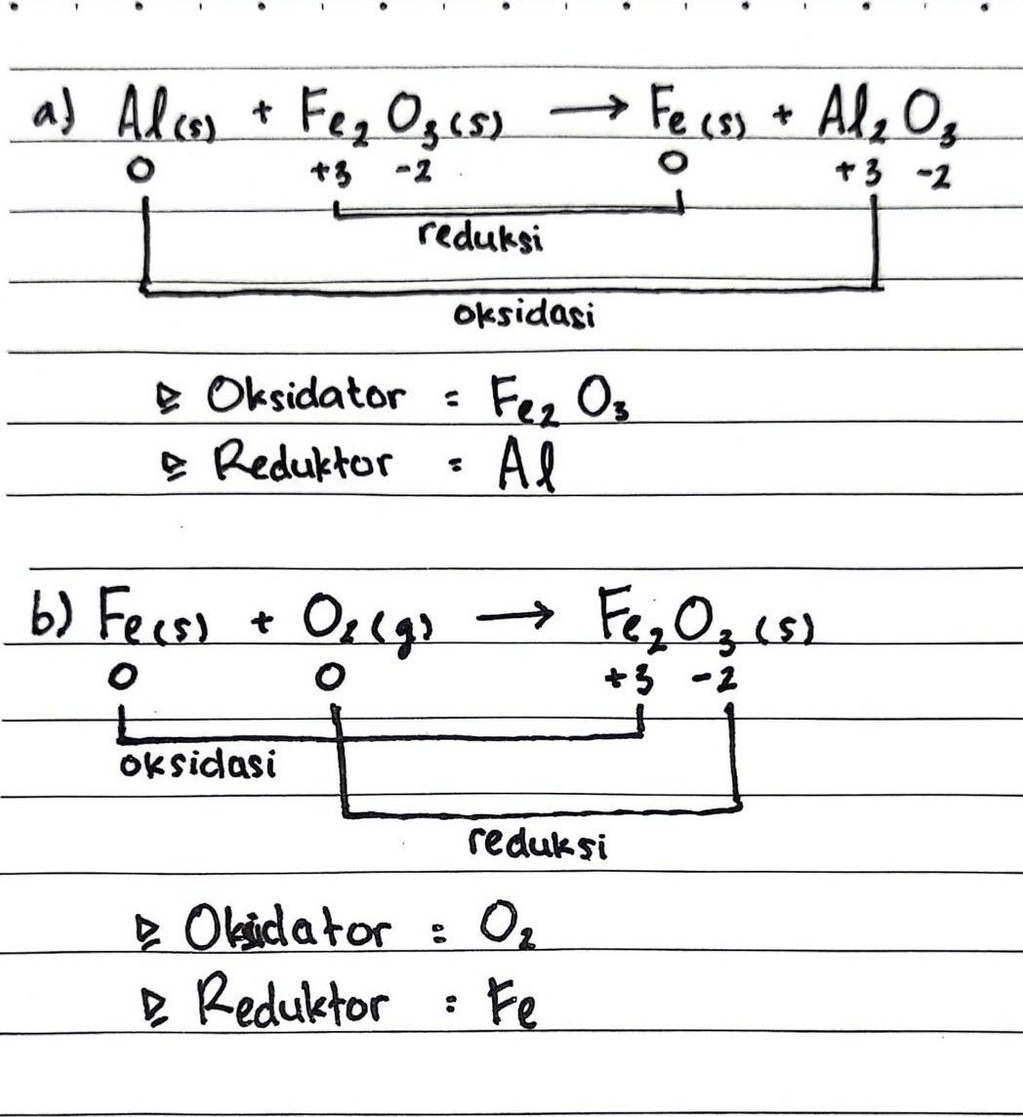
- Reaksi Reduksi : zat yang mengalami penurunan bilangan oksidasi
- Reaksi Oksidasi : zat yang mengalami kenaikan bilangan oksidasi
Pengertian reduktor dan oksidator
- Reduktor : zat yang mereduksi atau yang mengalami oksidasi
- Oksidator : zat yang mengoksidasi atau yang mengalami reduksi
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



