Esther E
15 Januari 2023 05:58
Iklan
Esther E
15 Januari 2023 05:58
Pertanyaan
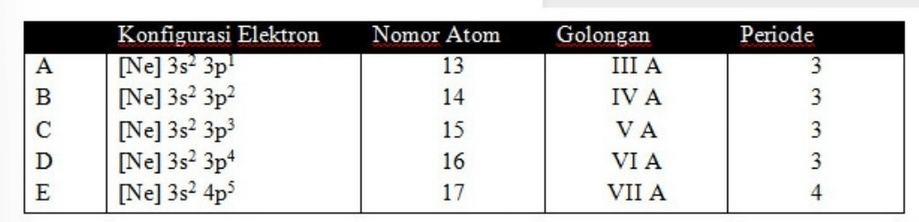
Konfigurasi elektron, nomor atom, dan letak unsur tersebut dalam sistem periodik yang paling tepat adalah ... (nomor atom Ne = 10)
3
1
Iklan
S. Susanti
Master Teacher
Mahasiswa/Alumni Universitas Jayabaya
31 Januari 2023 09:53
<p>Jawaban : benar semua kecuali E.</p><p> </p><p>Letak suatu unsur dalam sistem periodik dapat ditentukan berdasarkan konfigurasi elektronnya. Elektron valensi menunjukkan nomor golongan, sedangkan jumlah kulit (n) menunjukkan periode. Elektron valensi merupakan elektron yang terletak pada kulit terakhir dalam konfigurasi elektron yang digunakan untuk berikatan.</p><p> </p><p>Pada unsur golongan utama (A), golongan IA dan IIA memiliki elektron valensi yang berakhiran pada subkulit ns<sup>x</sup>, sementara golongan IIIA - VIIIA memiliki elektron valensi yang berakhiran pada (ns<sup>x</sup> np<sup>y</sup>). Unsur golongan transisi (B) memiliki elektron valensi yang berakhiran pada ns<sup>x</sup> (n-1)d<sup>y</sup>. Jika jumlah dari x dan y adalah 8, 9, 10 maka unsur tersebut termasuk ke dalam golongan VIIIB, sedangkan jika jumlahnya 11 berarti golongan IB, dan jika jumlahnya 12 maka termasuk golongan IIB. Urutan pengisian elektron pada orbital berdasarkan konfigurasi Aufbau adalah seperti pada gambar (terlampir).</p><p> </p><p>Jika nomor atom unsur X diatas adalah 17, maka konfigurasinya elektronnya yaitu:</p><p>17X = 1s<sup>2</sup> 2s<sup>2</sup> 2p<sup>6</sup> 3s<sup>2</sup> 3p<sup>5</sup></p><p>Jika digunakan peringkasan konfigurasi elektron gas mulia, maka:</p><p>17X = [Ne] 3s<sup>2</sup> 3p<sup>5</sup></p><p>Pada konfigurasi elektron diatas, elektron valensinya berakhiran pada 3s<sup>2</sup> 3p<sup>5</sup> maka:</p><p>• periode = jumlah kulit = 3</p><p>• golongan = elektron valensi = 2 + 5 = 7 sehingga termasuk ke dalam golongan VIIA.</p><p>Pada soal di atas, opsi E tidak sesuai karena konfigurasi elektron dan periodenya salah.<br> </p><p>Jadi, konfigurasi elektron, nomor atom, dan letak unsur tersebut dalam sistem periodik yang paling tepat adalah benar semua kecuali E.</p>
Jawaban : benar semua kecuali E.
Letak suatu unsur dalam sistem periodik dapat ditentukan berdasarkan konfigurasi elektronnya. Elektron valensi menunjukkan nomor golongan, sedangkan jumlah kulit (n) menunjukkan periode. Elektron valensi merupakan elektron yang terletak pada kulit terakhir dalam konfigurasi elektron yang digunakan untuk berikatan.
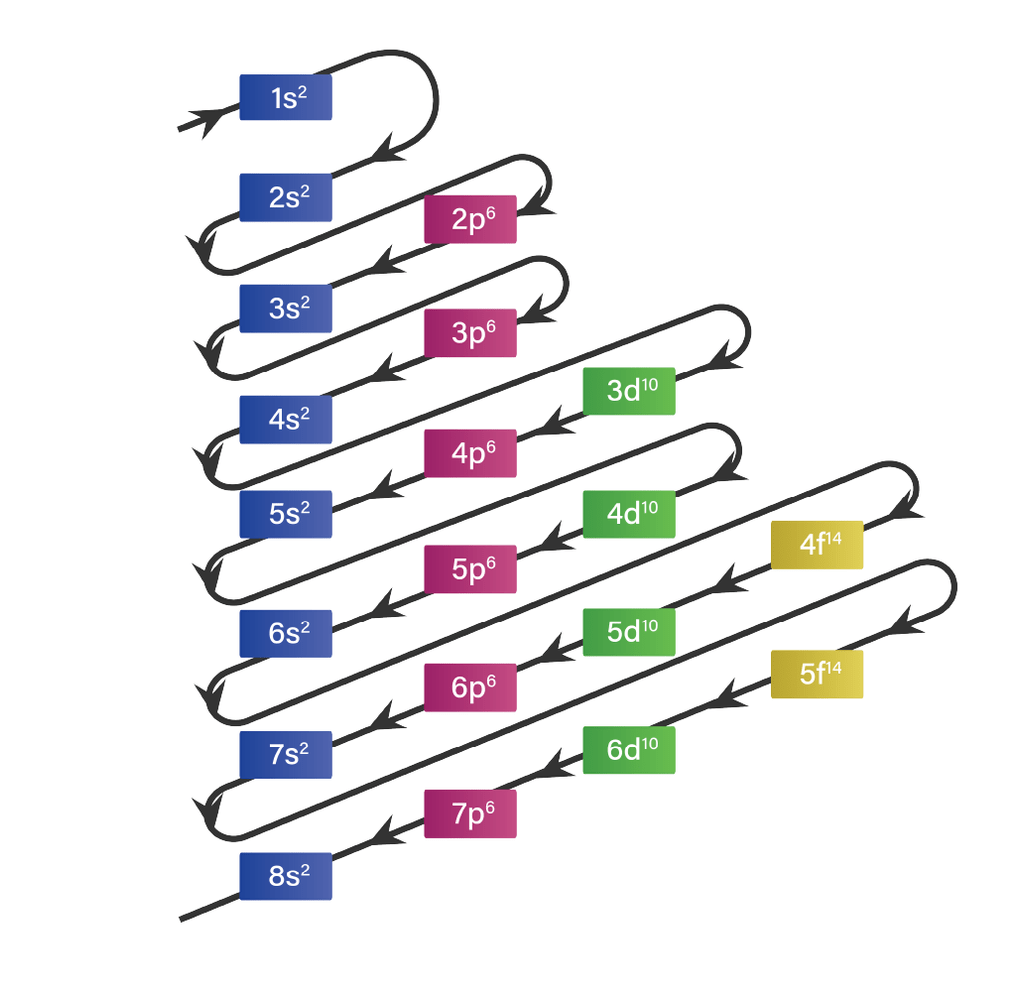
Pada unsur golongan utama (A), golongan IA dan IIA memiliki elektron valensi yang berakhiran pada subkulit nsx, sementara golongan IIIA - VIIIA memiliki elektron valensi yang berakhiran pada (nsx npy). Unsur golongan transisi (B) memiliki elektron valensi yang berakhiran pada nsx (n-1)dy. Jika jumlah dari x dan y adalah 8, 9, 10 maka unsur tersebut termasuk ke dalam golongan VIIIB, sedangkan jika jumlahnya 11 berarti golongan IB, dan jika jumlahnya 12 maka termasuk golongan IIB. Urutan pengisian elektron pada orbital berdasarkan konfigurasi Aufbau adalah seperti pada gambar (terlampir).
Jika nomor atom unsur X diatas adalah 17, maka konfigurasinya elektronnya yaitu:
17X = 1s2 2s2 2p6 3s2 3p5
Jika digunakan peringkasan konfigurasi elektron gas mulia, maka:
17X = [Ne] 3s2 3p5
Pada konfigurasi elektron diatas, elektron valensinya berakhiran pada 3s2 3p5 maka:
• periode = jumlah kulit = 3
• golongan = elektron valensi = 2 + 5 = 7 sehingga termasuk ke dalam golongan VIIA.
Pada soal di atas, opsi E tidak sesuai karena konfigurasi elektron dan periodenya salah.
Jadi, konfigurasi elektron, nomor atom, dan letak unsur tersebut dalam sistem periodik yang paling tepat adalah benar semua kecuali E.
· 0.0 (0)
Iklan
Buka akses jawaban yang telah terverifikasi

Yah, akses pembahasan gratismu habis
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia













