RC
Rafaela C
11 Agustus 2020 17:45
Iklan
RC
Rafaela C
11 Agustus 2020 17:45
Pertanyaan
Bagaimana cara penyetaraan NaCrO2 + Br2 + NaOH -> Na2CrO4 + NaBr + H2O
5
1
Iklan
MB
M. Bimba
Mahasiswa/Alumni Universitas Sanata Dharma
02 Januari 2022 15:27
Jawaban terverifikasi
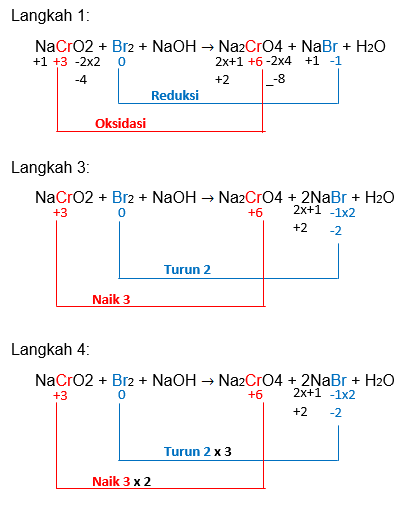
Halo Rafaela C, penyetaraan reaksi tersebut dapat dilakukan dengan metode bilangan oksidasi, maka reaksi setara yang didapatkan adalah 2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O Ayo simak penjelasan berikut, supaya kamu lebih paham. ^^ Reaksi redoks ialah reaksi yang terjadi karena adanya perubahan bilangan oksidasi. Oleh sebab itu reaksi redoks dapat disebut juga gabungan antara reaksi reduksi dan oksidasi. Dimana reaksi reduksi adalah reaksi akibat penurunan biloks, sedangkan reaksi oksidasi adalah reaksi akibat kenaikan biloks. Pada reaksi redoks, penyetaraan reaksi dapat dilakukan dengan dua cara yaitu metode bilangan oksidasi dan metode setengah reaksi. Pada reaksi yang diketahui, penyetaraan yang dapat dilakukan adalah metode setengah reaksi. Oleh sebab itu, tahapan yang dilakukan yaitu: • Menentukan unsur yang mengalami perubahan bilangan oksidasi yang dapat dilihat pada gambar (Terlampir). • Menyetarakan jumlah unsur yang mengalami perubahan biloks. Pada reaksi redoks tersebut, unsur yang mengalami perubahan biloks adalah unsur Cr dan Br. Jumlah unsur Cr pada ruas kiri sama dengan ruas kanan yaitu satu, sedangkan jumlah unsur Br pada ruas kiri 2 dan pada ruas kanan hanya 1. Maka, untuk menyetarakannya senyawa NaBr pada ruas kanan harus ditambahkan koefisien yaitu 2. Jadi, reaksinya menjadi NaCrO2 + Br2 + NaOH → Na2CrO4 + 2NaBr + H2O • Menentukan besarnya kenaikan dan penurunan biloks dari unsur yang mengalami perubahan biloks. Pada langkah ini, dapat dilihat pada gambar (Terlampir). • Menyetarakan perubahan biloks dengan cara perkalian silang untuk mendapatkan koefisien yang tepat dapat dilihat pada gambar (Terlampir). Oleh sebab itu, reaksi yang didapatkan yaitu: 2NaCrO2 + 3Br2 + NaOH → 2Na2CrO4 + 6NaBr + H2O • Menyetarakan unsur H, dan O serta unsur lainnya. Pada reaksi berikut: 2NaCrO2 + 3Br2 + NaOH → 2Na2CrO4 + 6NaBr + H2O Jumlah unsur Na dan H belum setara. Oleh sebab itu, kedua unsur tersebut perlu ditambahkan koefisien. Unsur Na Jumlah unsur Na pada ruas kiri 3, sedangkan pada ruas kanan 10. Maka, senyawa NaOH harus ditambahkan koefisien yaitu 8, maka reaksi yang diperoleh sebagai berikut: 2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + H2O Unsur H Mengacu pada reaksi setelah penambahan koefisien NaOH, jumlah unsur H pada ruas kiri 8, sedangkan pada ruas kanan hanya 2. Maka, pada senyawa H2O harus ditambahkan koefisien yaitu 4. Dengan demikian, reaksi setara dan lengkap yang diperoleh sebagai berikut: 2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O Semoga penjelasan diatas bermanfaat ya, selamat belajar. ^^
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!
Roboguru Plus
Dapatkan pembahasan soal ga pake lama, langsung dari Tutor!


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



