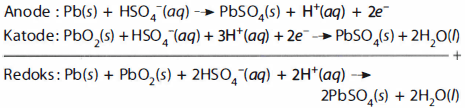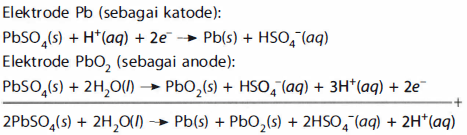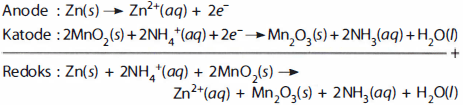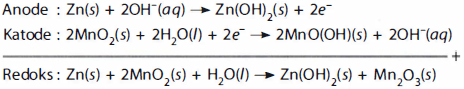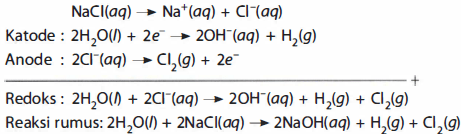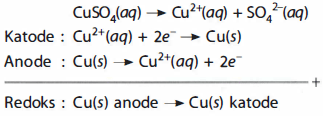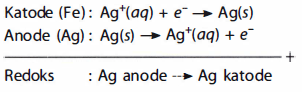Aplikasi sel volta:
a. Aki
Aki adalah jenis baterai yang banyak digunakan untuk kendaraan bermotor. Sel aki terdiri atas anode Pb (timbal = timah hitam) dan katode  (timbal(IV) oksida). Reaksi pengosongan aki adalah sebagai berikut:
(timbal(IV) oksida). Reaksi pengosongan aki adalah sebagai berikut:
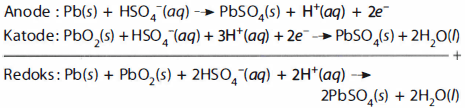
Aki dapat diisi ulang, berikut adalah reaksi pengisian ulang aki:
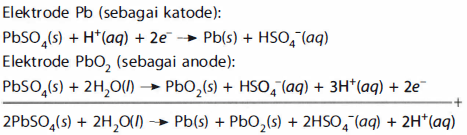
b. Baterai kering
baterai kering terdiri atas suatu silinder zink yang berisi pasta dari campuran batu kawi ( ), salmiak (
), salmiak ( ), karbon (C), dan sedikit air. Reaksi yang terjadi adalah:
), karbon (C), dan sedikit air. Reaksi yang terjadi adalah:
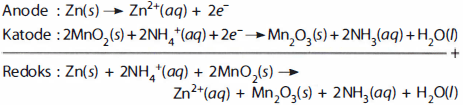
c. Baterai alkaline
Baterai kering alkaline pada dasarnya sama dengan baterai kering diatas, tetapi bersifat basa karena menggunakan  menggantikan
menggantikan  dalam pasta. Reaksi yang terjadi:
dalam pasta. Reaksi yang terjadi:
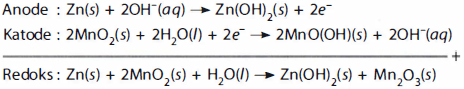
Aplikasi sel elektrolisis:
a. Produksi zat
Banyak zat kimia dibuat melalui elektrolisis, misalnya logam-logam alkali, magnesium, aluminium, fluorin, klorin, natrium hidroksida, natrium hipoklorit, dan hidrogen peroksida. Berikut adalah salah satu contoh elektrolisis larutan  menghasilkan
menghasilkan  di katode dan
di katode dan  di anode:
di anode:
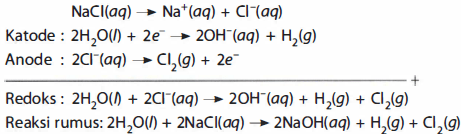
b. Pemurnian logam
Misalnya pada tembaga yang dimurnikan secara elektrolisis. Tembaga kotor dijadikan anode, sedangkan pada katode digunakan tembaga murni. Larutan elektrolit yang digunakan adalah larutan  . Reaksinya adalah sebagai berikut:
. Reaksinya adalah sebagai berikut:
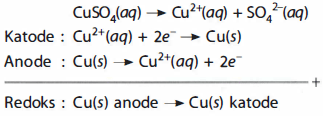
c. Penyepuhan
Penyepuhan bertujuan untuk melindungi logam terhadap korosi atau untuk memperbaiki penampilan. Logam yang akan disepuh dijadikan katode, sedangkan logam penyepuhnya sebagai anode. Kedua elektrode tersebut dicelupkan dalam larutan garam dari logam penyepuh. Contoh, penyepuhan sendok yang terbuat dari besi (baja) dengan perak.
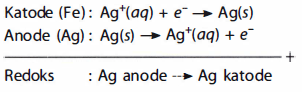
Jadi, aplikasi sel volta adalah pada aki, baterai kering, baterai alkaline. Sedangkan aplikasi sel elektrolisis adalah produksi zat, pemurnian logam, dan penyepuhan.