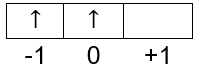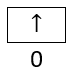Bilangan kuantum adalah bilangan yang digunakan sebagai penentu kedudukan elektron dalam atom. Terdapat 4 jenis bilangan kuantum yaitu:
- Bilangan kuantum utama (n), yang menunjukkan kulit atom,
- bilangan kuantum azimuth (l), yang menunjukkan subkulit atom,
- bilangan kuantum magnetik (m), yang menunjukkan jumlah orbital, dan
- bilangan kuantum spin (s), yang menunjukkan orientasi elektron terhadap medan magnet di sekitarnya.
Dalam penentuan bilangan kuantum pada suatu unsur perlu untuk menentukan konfigurasi elektronnya terlebih dahulu agar dapat mengetahui elektron terakhir atom tersebut.
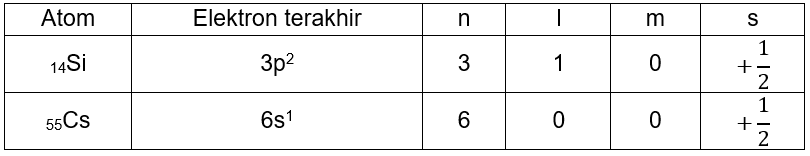
Konfigurasi elektron dan penentuan elektron terakhir 14Si dan 55Cs
14Si=[Ne]3s23p2 (elektron terakhirnya adalah 3p2)
55Cs=[Xe]6s1 (elektron terakhirnya adalah 6s1)
Penentuan bilangan kuantum 14Si dan 55Cs
Elektron terakhir 14Si adalah 3p2 sehingga:
n= 3 (terletak pada kulit ke-3)
l= 1 karena elektron terakhirnya pada subkulit p, maka l-nya bernilai 1
m= subkulit p memiliki 3 orbital yang masing-masing orbitalnya dapat terisi maksimal 2 elektron dan pengisian elektron dimulai dari yang tidak berpasangan terlebih dahulu. Maka diagram orbital untuk 3p2 adalah:
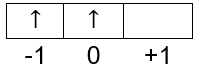
Elektron terakhir berhenti pada orbital bernomor 0, oleh karena itu nilai m= 0
s= +21, karena elektron terakhir pada diagram orbital ke arah atas, maka nilai bilangan kuantum spinnya adalah +21
Elektron terakhir 55Cs adalah 6s1 sehingga:
n= 6 (terletak pada kulit ke-6)
l= 0 karena elektron terakhirnya pada subkulit s, maka l-nya bernilai 0
m= subkulit s memiliki 1 orbital yang dapat terisi maksimal 2 elektron dan pengisian elektron dimulai dari yang tidak berpasangan terlebih dahulu. Maka diagram orbital untuk 6s1 adalah:
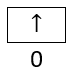
Elektron terakhir berhenti pada orbital bernomor 0, oleh karena itu nilai m= 0
s= +21, karena elektron terakhir pada diagram orbital ke arah atas, maka nilai bilangan kuantum spinnya adalah +21.
Jadi, bilangan kuantum elektron terakhir 14Si dan 55Cs adalah: