Iklan
Pertanyaan
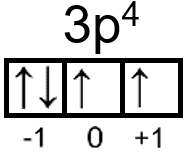
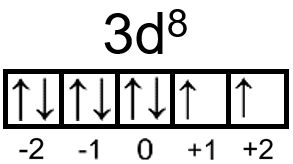
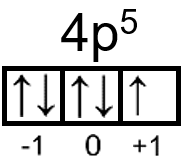
Tentukan bilangan kuantum unsur-unsur berikut! a. 16 S b. 28 Ni c. 35 Br
Tentukan bilangan kuantum unsur-unsur berikut!
a.
b.
c.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
15
4.8 (5 rating)
NM
Nawfal Muchtar
Mudah dimengerti
HK
Hermiaty Kaissi
Pembahasan lengkap banget
0
000000000000000000000000f36486a95a9dc3c93a4c1f41bf0deaf825dc6d21d45c2c1aca768ea77e727610fc
Pembahasan lengkap banget Ini yang aku cari! Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia