Iklan
Pertanyaan
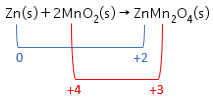
Suatu sel kering bekerja menurut reaksi berikut. Zn ( s ) + 2 MnO 2 ( s ) → ZnMn 2 O 4 ( s ) Untuk menghasilkan muatan sebesar 965 Coulomb, kondisi yang tepat adalah .... ( A r O = 16, Mn = 55,dan Zn = 65)
Suatu sel kering bekerja menurut reaksi berikut.
Untuk menghasilkan muatan sebesar 965 Coulomb, kondisi yang tepat adalah .... (O = 16, Mn = 55, dan Zn = 65)
jumlah Zn yang bereaksi adalah 0,65 g
jumlah
yang bereaksi adalah 0,435 g
jumlah
yang terbentuk adalah 0,005 mol
bertindak sebagai reduktor
Zn digunakan sebagai katoda
Iklan
SI
S. Ibabas
Master Teacher
Jawaban terverifikasi
6
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia