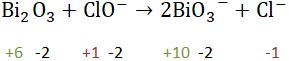Penyetaraan persamaan reaksi redoks dengan metode bilangan oksidasi dilakukan dengan menyamakan jumlah elektron yang dilepaskan oleh reduktor dan elektron yang diikat oleh oksidator. Perubahan bilangan oksidasi besarnya sama dengan jumlah elektron yang terlibat.
Langkah pertama dalam menyetarakan reaksi redoks dengan metode biloks adalah menentukan biloks masing-masing atom pada reaksi. Menyetarakan atom yang mengalami perubahan bilangan oksidasi.
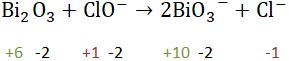
Kemudian menentukan jumlah penurunan dan kenaikan bilangan oksidasi. Samakan perubahan tersebut dengan cara mengali jumlah atom dalam zat tersebut agar perubahan biloksnya sama.
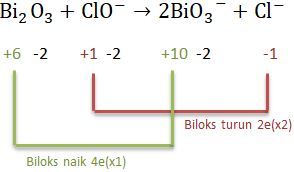
Jika perubahan biloks dikali, maka koefisien reaksi juga dikalikan dengan bilangan yang sama, sehingga persamaan reaksi menjadi:

Langkah berikutnya kita samakan atom O dan H dengan menambahkan  pada sisi yang kelebihan O, dan menambahkan
pada sisi yang kelebihan O, dan menambahkan  pada sisi yang berlawanan sebanyak dua kali lipat penambahan
pada sisi yang berlawanan sebanyak dua kali lipat penambahan  (suasana basa).
(suasana basa).

Jadi, persamaan reaksi setaranya adalah
 .
.
Metode Ion Eletron
Metode setengah reaksi didasarkan pada pengertian bahwa jumlah elektron yang dilepaskan pada setengah reaksi oksidasi sama dengan jumlah elektron yang diserap pada setengah reaksi reduksi. Penyetaraan dalam larutan bersuasana basa berbeda dengan suasana asam. Penyetaraan larutan basa menggunakan langkah penyetaraan sebagai berikut:
Langkah pertama dalam penyetaraan reaksinya adalah dengan menuliskan kerangka dasar dari setengah reaksi reduksi dan setengah reaksi oksidasi secara terpisah dalam bentuk reaksi ion.

Langkah kedua, masing-masing reaksi setengah reaksi disetarakan dengan urutan sebagai berikut.
- Setarakan atom unsur yang mengalami perubahan bilangan oksidasi (biasanya adalah unsur selain oksigen dan hidrogen).
- Setarakan oksigen dengan menambahkan molekul air (
 ).
).
- Setarakan atom hidrogen dengan menambahkan ion
 .
.
- Menghilangakn ion
 dengan menambahkan ion
dengan menambahkan ion  pada kedua ruas.
pada kedua ruas.
- Setarakan muatan dengan menambahkan elektron.


Samakan jumlah elektron yang diserap pada setengah reaksi reduksi dengan jumlah elektron yang dibebaskan pada setengah reaksi oksidasi dengan cara memberi koefisien yang sesuai, kemudian jumlahkan kedua setengah reaksi tersebut.

Jadi, reaksi redoks setaranya adalah  .
.