Pada penyetaraan reaksi kimia, jumlah atom pada ruas kiri dan ruas kanan harus sama. Langkah yang digunakan untuk penyetaraan reaksi kimia yaitu:
1. Pemberian koefisien reaksi pada setiap zat

2. Penentuan persamaan matematika berdasarkan unsur yang sama
 (1)
(1)
 (2)
(2)
3. Perhitungan koefisien a, b, dan c
Perhitungan koefisien a, b, dan c dilakukan dengan melakukan pemisalan pada salah satu koefisien, misal a=1, maka :


3. Nilai koefiesien yang telah diperoleh disubtitusikan ke persamaan reaksi kimia

Koefisien persamaan reaksi diatas berbentuk pecahan, agar koefisien reaksi tidak berbentuk pecahan maka koefisien dikalikan dengan 2. Persamaan reaksinya adalah sebagai berikut:

4. Pemeriksaan jumlah atom di ruas kiri dan kanan
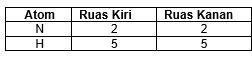
Tabel diatas menunjukkan bahwa jumlah atom diruas kiri dan kanan sudah setara, sehingga persamaan reaksi sudah setara.
Jadi, persamaan reaksi yang yang sudah setara adalah sebagai berikut:



















