Soal diatas merupakan reaksi oksidasi dan reduksi. Oleh karena itu, kita tentukan dahulu spesi yang mengalami oksidasi dan reduksi menggunakan perubahan bilangan oksidasi. Jika terjadi kenaikan biloks, spesi mengalami oksidasi sedangkan jika terjadi penurunan biloks, spesi akan mengalami reduksi.
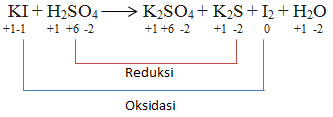
Selanjutnya, penyetaraan dapat dilakukan menggunakan metode setengah reaksi.
- Setengah reaksi untuk reduksi

Kekurangan atom K di sebelah kiri dapat ditambahkan dengan spesi KI. Selanjutnya di sebelah kananperlu ditambah  untuk kekurangan atom I.
untuk kekurangan atom I.

Kemudian, koefisien KI menjadi 2 untuk menyetarakan atom K dan I.

Kekurangan H disebelah kanan dapat ditambahkan  dan selanjutnya disetarakan jumlah atom H dengan penambahan ion
dan selanjutnya disetarakan jumlah atom H dengan penambahan ion  .
.

- Setengah reaksi untuk oksidasi

Karena spesi K tidak ada di sebelah kanan, maka dapat ditambahkan  . Selanjutnya, kekurangan ion sulfat disebelah kiri, dapat diantisipasi dengan penambahan
. Selanjutnya, kekurangan ion sulfat disebelah kiri, dapat diantisipasi dengan penambahan  .
.

Jumlah atom K dan I disetarakan dengan menambah koefisien KI menjadi 2. Kemudian, ditambahkan 2 ion  untuk menyamakan atom H serta menambahkan 2 elektron untuk menyamakan muatan kedua bagian.
untuk menyamakan atom H serta menambahkan 2 elektron untuk menyamakan muatan kedua bagian.

Selanjutnya dikalikan 3, untuk mengeliminasi elektron dan ion hidrogen dalam persamaan reaksi di atas.

- Menjumlahkan reaksi oksidasi dan reduksi

Jadi, reaksi yang setara adalah
 .
.















