Iklan
Pertanyaan
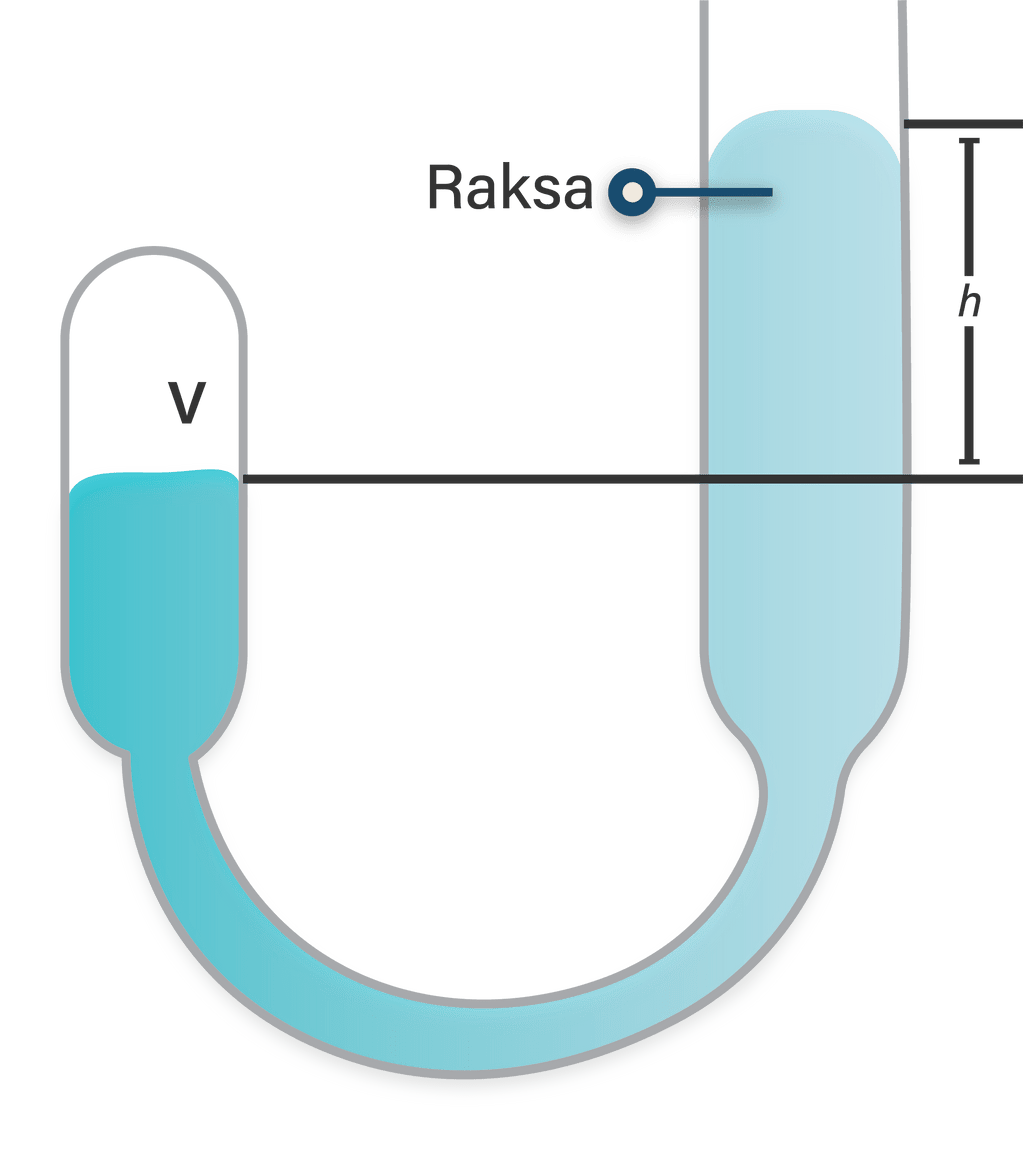
Seorang siswa ingin menerapkan hukum Boyle untuk menentukan tekanan udara luar. Ia menggunakan peralatan seperti pada gambar di bawah. Ia mendapatkan bahwa ketika h = 50 mm, V = 18 cm 3 dan ketika h = 150 mm, V = 16 cm 3 . Berapakah tekanan udara luar di tempat siswa itu melakukan percobaan? Nyatakan dalam mmHg.
Seorang siswa ingin menerapkan hukum Boyle untuk menentukan tekanan udara luar. Ia menggunakan peralatan seperti pada gambar di bawah. Ia mendapatkan bahwa ketika h = 50 mm, V = 18 cm3 dan ketika h = 150 mm, V = 16 cm3. Berapakah tekanan udara luar di tempat siswa itu melakukan percobaan? Nyatakan dalam mmHg.
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia

















