Proses hantaran listrik pada senyawa ionik adalah ketika ion-ion terurai dan bergerak bebas.
Larutan yang dapat menghantarkan listrik disebut sebagai larutan elektrolit. Larutan elektrolit dapat menghantarkan listrik karena mengandung ion-ion yang dapat bergerak bebas. Ion-ion itulah yang menghantar arus listrik melalui larutan.
Senyawa ionik adalah senyawa yang terbentuk dari ion melalui ikatan ionik. Ion-ion penyusun senyawa ionik terdiri atas ion positif dan ion negatif. Senyawa ionik dapat berada dalam keadaan padat, cair, atau larutan.
Senyawa ionik dalam bentuk padat tidak dapat menghantarkan listrik, karena ion-ionnya terikat sangat rapat dan kuat. Sedangkan senyawa ion dalam keadaan cair, memiliki jarak antar ion-ion yang renggang, sehingga ion-ion tersebut dapat menghantarkan listrik. Jika senyawa ionik dilarutkan dalam air, ion ion tersebut akan terurai oleh air dan bergerak bebas sehingga larutan ini juga dapat menghantarkan arus listrik.
Contohnya adalah pada senyawa NaCl, reaksi dan proses pengionan larutan garam seperti pada gambar di bawah ini.
NaCl(aq)→Na+(aq)+Cl−(aq)
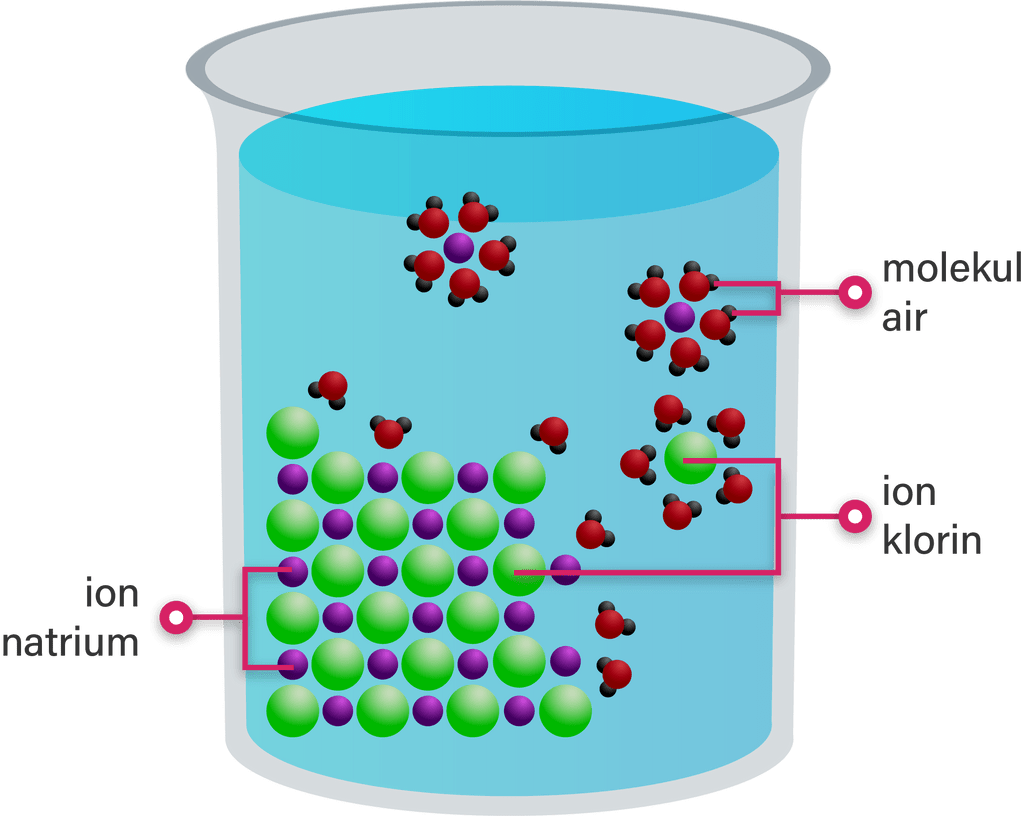
Dengan demikian, proses hantaran listrik pada senyawa ionik dimulai ketika ion-ion senyawa tersebut merenggang atau terurai sehingga ion-ionnya bergerak bebas, semakin banyak ion-ion yang terurai, semakin baik daya hantar cairan tersebut.
















