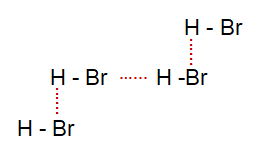Iklan
Pertanyaan
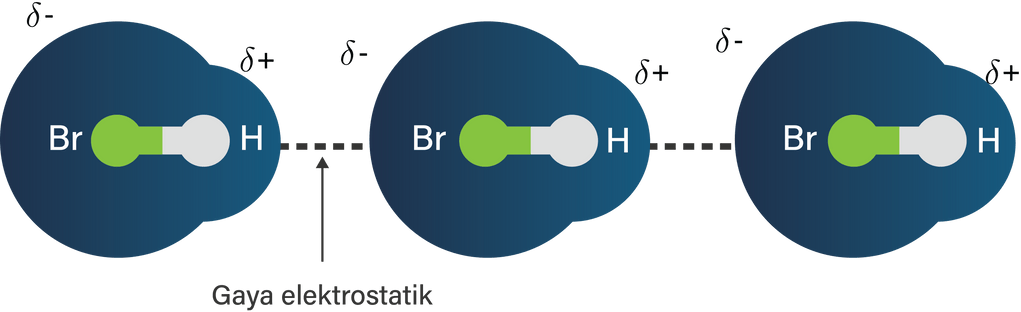
Senyawa HBr merupakan senyawa kovalen polar yang dapat mengalamigaya elektrostatik antarmolekul. Gambarkanlah gaya elektrostatikantarmolekul HBr yang terjadi.
Senyawa HBr merupakan senyawa kovalen polar yang dapat mengalami gaya elektrostatik antarmolekul. Gambarkanlah gaya elektrostatik antarmolekul HBr yang terjadi.
Iklan
NA
N. Agnia
Master Teacher
Mahasiswa/Alumni Institut Pertanian Bogor
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia