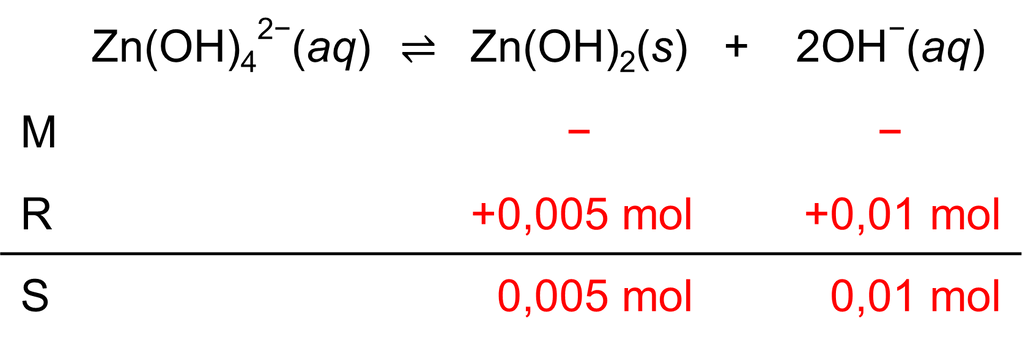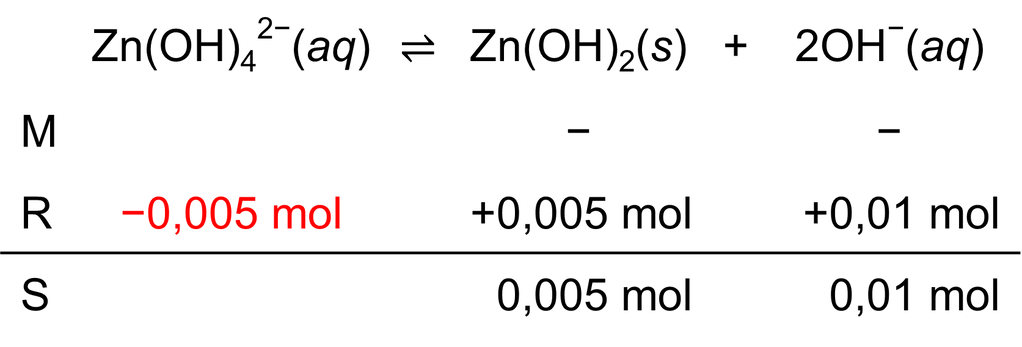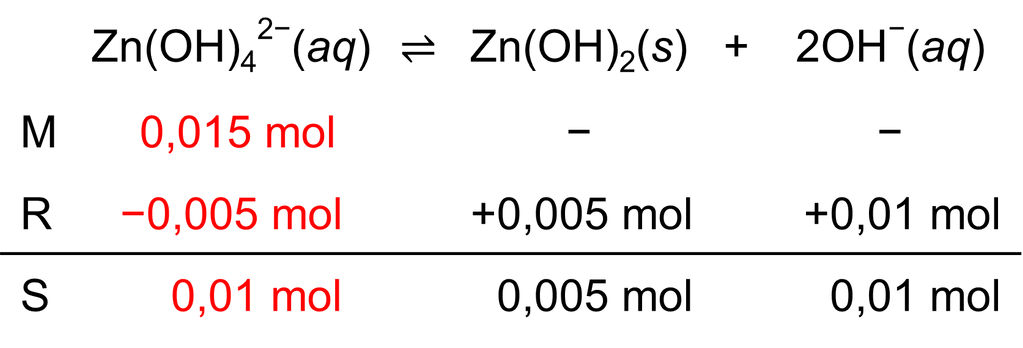Iklan
Pertanyaan
Seng hidroksida ( M r = 99 ) diperoleh dalam larutan basa dari disosiasi kompleks sesuai reaksi berikut. Zn ( OH ) 4 2 − ( a q ) ⇌ Zn ( OH ) 2 ( s ) + 2 OH − ( a q ) Saat K c bernilai 0,01, massa endapan terbentuk 0,495 g dengan konsentrasi ion hidroksida sebesar 0,01 M dalam 1 L larutan.Derajat disosiasi ion kompleks sebesar ....
Seng hidroksida diperoleh dalam larutan basa dari disosiasi kompleks sesuai reaksi berikut.
Saat bernilai 0,01, massa endapan terbentuk 0,495 g dengan konsentrasi ion hidroksida sebesar 0,01 M dalam 1 L larutan. Derajat disosiasi ion kompleks sebesar ....
33,33%
0,5%
50%
0,33%
25%
Iklan
SI
S. Ibabas
Master Teacher
Jawaban terverifikasi
3
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia