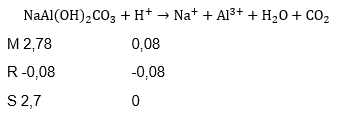Iklan
Pertanyaan
Sebuah tablet antasida mengandug 400 mg NaAl(OH) 2 CO 3 (Mr = 144 g mol -1 ). Tablet tersebut digunakan untuk mengurangi kadar HCl dalam lambung. Reaksi antara antasida dengan asam lambung dituliskan sebagai berikut. NaAl ( OH ) 2 CO 3 ( s ) + H + ( a q ) → Na + ( a q ) + Al 3 + ( a q ) + H 2 O ( l ) + CO 2 ( g ) Saat seseorang mengalami gangguan lambung,konsentrasi HCl dalam lambung sebesar 0,1 M. Jika lambung seseorang mengandung 800 mL HCl 0,1 M dan ia mengonsumsi 1 tablet antasida dengan 200 ml air, apakah konsentrasi HCI dalam lambungnya sudah mencapai keadaan normal? (Diasumsikan konsentrasi HCl dalam lambung pada keadaan normal sekitar 0,08 M)
Sebuah tablet antasida mengandug 400 mg NaAl(OH)2CO3 (Mr = 144 g mol-1). Tablet tersebut digunakan untuk mengurangi kadar HCl dalam lambung. Reaksi antara antasida dengan asam lambung dituliskan sebagai berikut.
Saat seseorang mengalami gangguan lambung,konsentrasi HCl dalam lambung sebesar 0,1 M. Jika lambung seseorang mengandung 800 mL HCl 0,1 M dan ia mengonsumsi 1 tablet antasida dengan 200 ml air, apakah konsentrasi HCI dalam lambungnya sudah mencapai keadaan normal? (Diasumsikan konsentrasi HCl dalam lambung pada keadaan normal sekitar 0,08 M)
Iklan
A. Tri
Master Teacher
Mahasiswa/Alumni Universitas Pertamina
4
4.4 (5 rating)
Alfina Gusti Damayanti
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia