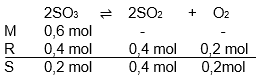Iklan
Pertanyaan
Sebanyak 0,6 mol SO 3 dimasukkan ke dalam ruang tertutup pada suhu 32 7 ∘ C dan dibiarkan terdisosiasi dalam volume 2 L 2 SO 3 ( g ) ⇌ 2 SO 2 ( g ) + O 2 ( g ) pada saat setimbang diketahui berdisosiasi 66 , 67% , besarnya Kcdan Kp ...
Sebanyak 0,6 mol dimasukkan ke dalam ruang tertutup pada suhu dan dibiarkan terdisosiasi dalam volume 2 L
pada saat setimbang diketahui berdisosiasi , besarnya Kc dan Kp ...
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia