Iklan
Pertanyaan
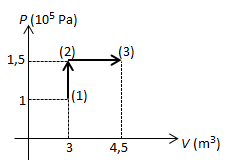
Sebanyak 0,42 mol gas ideal monoatomik dengan tekanan 10 5 Pa, volume 3 m 3 , dan suhu 300 K. Mula-mula gas mengalami proses isokhorik sehingga tekanannya menjadi 1 , 5 × 1 0 5 Pa . Gas mengalami proses isobarik hingga volumenya menjadi 4,5 m 3 . Kapasitas kalor gas monoatomik pada volume tetap C V = 2 3 n R . Hitung kalor total yang diserap oleh gas.
Sebanyak 0,42 mol gas ideal monoatomik dengan tekanan 105 Pa, volume 3 m3, dan suhu 300 K. Mula-mula gas mengalami proses isokhorik sehingga tekanannya menjadi . Gas mengalami proses isobarik hingga volumenya menjadi 4,5 m3. Kapasitas kalor gas monoatomik pada volume tetap . Hitung kalor total yang diserap oleh gas.
Iklan
IF
I. Fitriatmoko
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
2
4.7 (4 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia