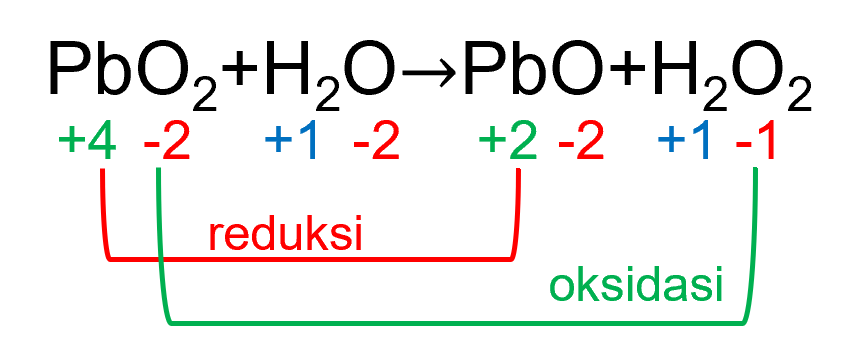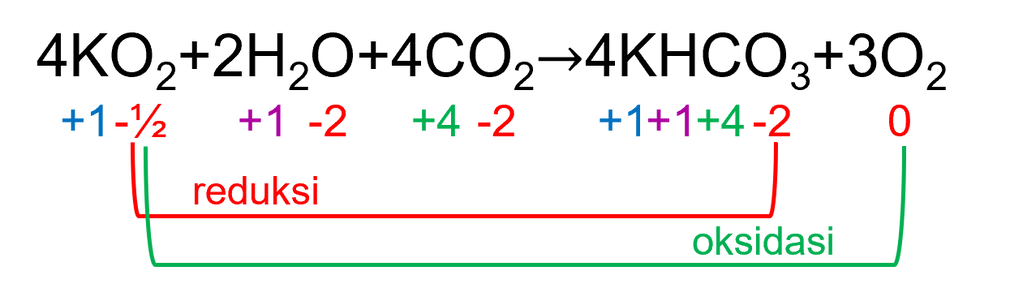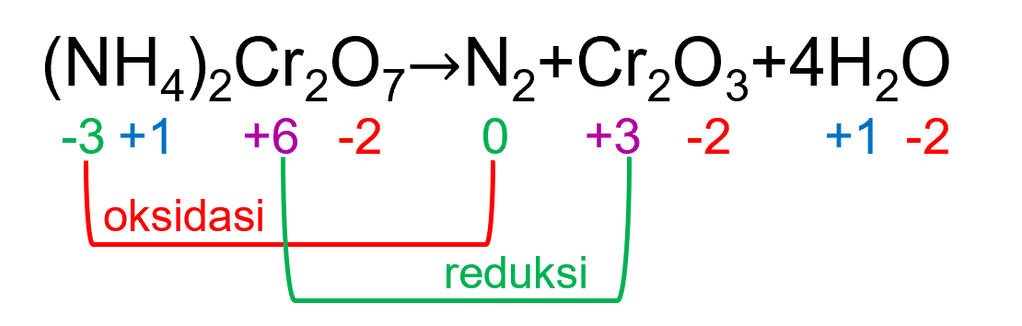Reaksi disproporsionasi atau reaksi autoredoks adalah salah satu jenis reaksi redoks dengan zat reduktor sama dengan oksidator. Pada reaksi reduksi dan oksidasi, unsur yang mengalami reduksi dan oksidasi sekaligus adalah unsur yang sama.
Berikut ini adalah analisis masing-masing reaksi di pilihan jawaban.
1. PbO2+H2O→PbO+H2O2
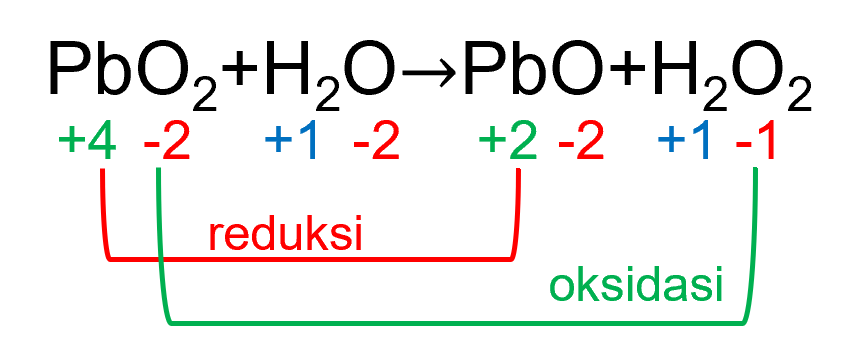
Berdasarkan gambar di atas, terlihat bahwa PbO2 mengalami reduksi dan oksidasi sekaligus atau bertindak sebagai reduktor dan oksidator. Akan tetapi, unsur yang mengalami reduksi dan oksidasi tidak sama. Unsur Pb mengalami reduksi, sedangkan unsur O mengalami oksidasi. Dengan demikian, reaksi di atas bukan merupakan reaksi disproporsionasi. (Reaksi 1 BENAR)
2. 4KO2+2H2O+4CO2→4KHCO3+3O2
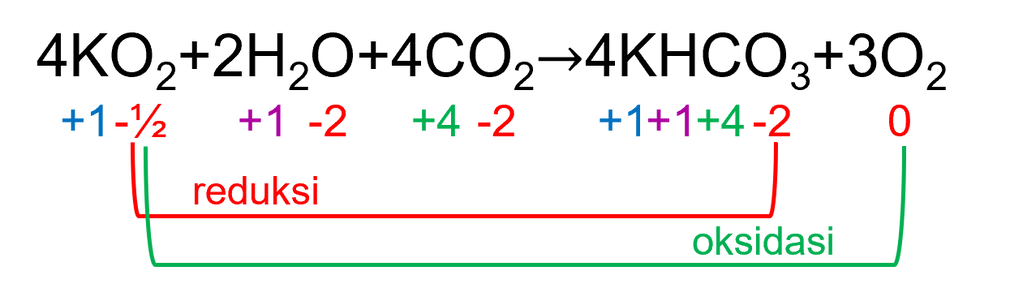
Berdasarkan gambar di atas, terlihat bahwa KO2 mengalami reduksi dan oksidasi sekaligus atau bertindak sebagai reduktor dan oksidator. Dalam hal ini, unsur yang mengalami reduksi dan oksidasi adalah unsur yang sama, yaitu O. Dengan demikian, reaksi di atas merupakan reaksi disproporsionasi. (Reaksi 2 SALAH)
3. (NH4)2Cr2O7→N2+Cr2O3+4H2O
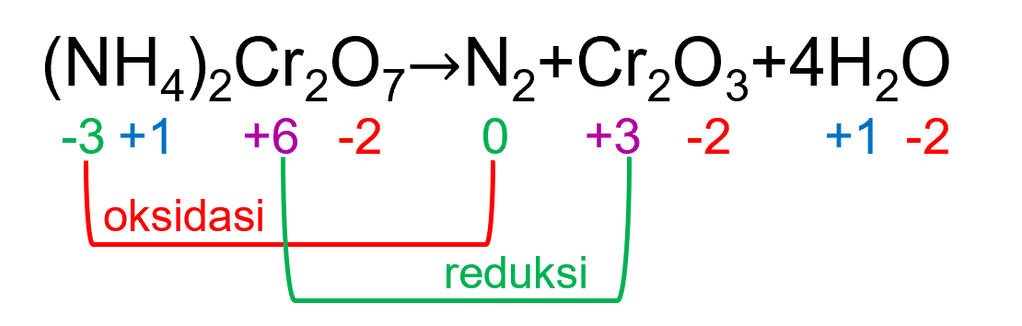
Berdasarkan gambar di atas, terlihat bahwa (NH4)2Cr2O7 mengalami reduksi dan oksidasi sekaligus atau bertindak sebagai reduktor dan oksidator. Akan tetapi, unsur yang mengalami reduksi dan oksidasi tidak sama. Unsur N mengalami oksidasi, sedangkan unsur Cr mengalami oksidasi. Dengan demikian, reaksi di atas bukan merupakan reaksi disproporsionasi. (Reaksi 3 BENAR)
4. 3Cl2+6NaOH→5NaCl+NaClO3+3H2O
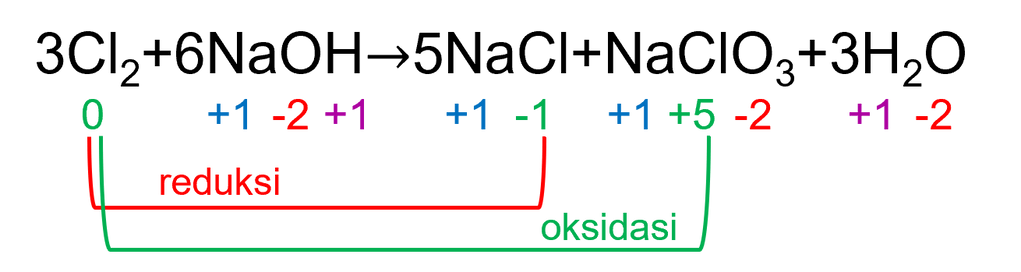
Berdasarkan gambar di atas, terlihat bahwa Cl2 mengalami reduksi dan oksidasi sekaligus atau bertindak sebagai reduktor dan oksidator. Dalam hal ini, unsur yang mengalami reduksi dan oksidasi adalah unsur yang sama, yaitu Cl. Dengan demikian, reaksi di atas merupakan reaksi disproporsionasi. (Reaksi 4 SALAH)
Alasan mengapa opsi jawaban yang salah bisa dipilih.
- Jika kurang teliti dalam membaca soal dan mengira bahwa yang ditanyakan adalah reaksi disproporsionasi, opsi C kemungkinan dipilih.
- Jika kurang teliti dalam membaca soal dan mengira bahwa yang ditanyakan adalah reaksi disproporsionasi dan juga tidak memahami dengan baik terkait reaksi disproporsionasi, opsi E kemungkinan dipilih.
- Tidak ada alasan khusus mengapa opsi A dan D bisa dipilih, kecuali mengawur dalam menjawab soal.
Jadi, jawaban yang tepat adalah B.