Iklan
Pertanyaan
HCl punya nilai K a = 1 0 5 , sedangkan K a dari H 2 O = 1 0 − 15 , berdasarkan fakta tersebut,pernyataan BENAR adalah ....
punya nilai , sedangkan dari berdasarkan fakta tersebut, pernyataan BENAR adalah ....
keasaman lemah
lebih daripada air
kebasaan
lebih kuat dari
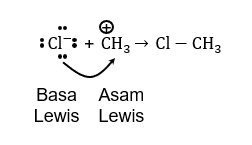
dapat menyerang karbokation
kurang stabil dibanding
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia