Iklan
Pertanyaan
Perhatikan tabel sistem periodik unsurberikut! Pernyataan yang tepat mengenai sifat keperiodikan keempatunsur tersebut adalah ...
Perhatikan tabel sistem periodik unsur berikut!
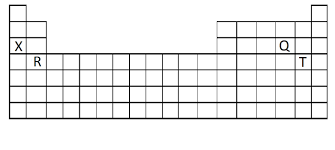
Pernyataan yang tepat mengenai sifat keperiodikan keempat unsur tersebut adalah ...
Jari-jari atom unsur X lebih besar dari unsur Q.
Energi ionisasi unsur T lebih kecil dari unsur R.
Unsur X memiliki kelektronegatifan paling besar.
Afinitas elektron unsur R lebih besar dari unsur T.
Unsur Q memiliki jari-jari atom paling besar.
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
5
1.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















