Iklan
Pertanyaan
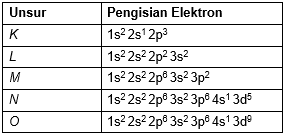
Perhatikan tabel pengisian elektron-elektron ke dalam subkulit berikut! Pengisian elektron yang benar menurut aturan Aufbau dan Hund terdapat pada nomor ...
Perhatikan tabel pengisian elektron-elektron ke dalam subkulit berikut!
Pengisian elektron yang benar menurut aturan Aufbau dan Hund terdapat pada nomor ...
K dan L
K dan M
L dan O
M dan N
N dan O
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
5
3.3 (3 rating)
A
Azizah
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia