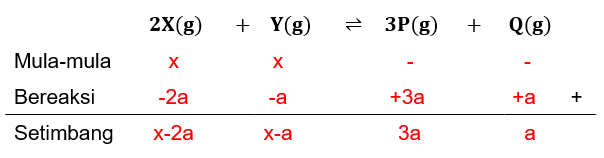Iklan
Pertanyaan
Perhatikan reaksi kesetimbangan: 2 X ( g ) + Y ( g ) ⇌ 3 P ( g ) + Q ( g ) Jika ke dalam suatu ruang hanya dimasukkan zat-zat X dan Y dengan jumlah mol yang sama, maka pada keadaan setimbang berlaku ....
Perhatikan reaksi kesetimbangan:
Jika ke dalam suatu ruang hanya dimasukkan zat-zat X dan Y dengan jumlah mol yang sama, maka pada keadaan setimbang berlaku ....
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
4
4.6 (6 rating)
C
Chayara
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Bantu banget Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia