Iklan
Pertanyaan
Perhatikan reaksi kesetimbangan berikut. aA ( g ) + bB ( g ) ⇌ cC ( g ) + dD ( g ) Jika tekanan parsial gas yang terlibat dalam reaksi berturut-turut P A, P B, P Cdan P D, buktikan bahwanilai kesetimbangan Kc dapat ditentukandengan persamaan: △ n = ( c + d ) − ( b + a ) (gunakan tetapan gas ideal, R = 0 , 082 L atm mol − 1 K − 1 )
Perhatikan reaksi kesetimbangan berikut.
Jika tekanan parsial gas yang terlibat dalam reaksi berturut-turut PA, PB, PC dan PD, buktikan bahwa nilai kesetimbangan Kc dapat ditentukan dengan persamaan:
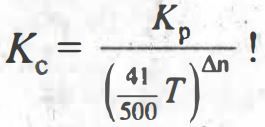
(gunakan tetapan gas ideal, R = )
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia

















