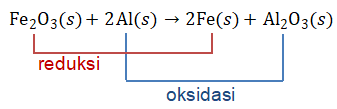Iklan
Pertanyaan
Perhatikan reaksi dan pernyataan berikut! Fe 2 O 3 ( s ) + 2 Al ( s ) → 2 Fe ( s ) + Al 2 O 3 ( s ) Dari reaksi berikut, pernyataan yang benar adalah ... Bilangan oksidasi Alberubah dari 0 menjadi +3. Spesi Fe 2 O 3 bertindak sebagai oksidator. Spesi Almengalami reaksi oksidasi. Spesi Fedan Al 2 O 3 secara berurutan merupakan hasil oksidasi dan hasil reduksi.
Perhatikan reaksi dan pernyataan berikut!
Dari reaksi berikut, pernyataan yang benar adalah ...
- Bilangan oksidasi Al berubah dari 0 menjadi +3.
- Spesi bertindak sebagai oksidator.
- Spesi Al mengalami reaksi oksidasi.
- Spesi Fe dan secara berurutan merupakan hasil oksidasi dan hasil reduksi.
1, 2, dan 3 SAJA yang benar.
1 dan 3 SAJA yang benar.
2 dan 4 SAJA yang benar.
HANYA 4 yang benar.
SEMUA pilihan benar.
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia