Iklan
Pertanyaan
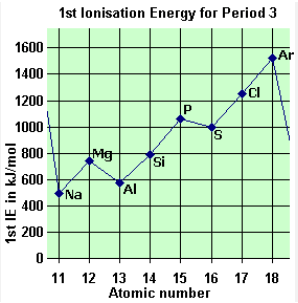
Perhatikan grafik berikut. Kecenderungan energi ionisasi unsur-unsur periode ketiga dari kiri ke kanan cenderung bertambah, namun terjadi penyimpangan pada energi ionisasi magnesium dan fosforus. Penyimpangan ini terjadi karena …
Perhatikan grafik berikut.
Kecenderungan energi ionisasi unsur-unsur periode ketiga dari kiri ke kanan cenderung bertambah, namun terjadi penyimpangan pada energi ionisasi magnesium dan fosforus. Penyimpangan ini terjadi karena
magnesium merupakan unsur logam sedangkan fosforus non logam
magnesium membentuk ikatan ionik sedangkan fosforus membentuk ikatan kovalen
magnesium dan fosforus mudah melepaskan elektron
magnesium dan fosforus mempunyai konfigurasi elektron yang relatif stabil
magnesium dan fosforus memiliki jari-jari atom yang besar
Iklan
N. Puspita
Master Teacher
3
4.4 (5 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia