Jadi, jawaban yang benar adalah D.
Korosi adalah adalah kerusakan atau kehancuran material akibat adanya reaksi kimia di sekitar lingkungannya. Korosi dapat dihambat dengan cara mengontrol atmosfer, mencegah logam bersinggungan dengan oksigen di udara dan juga air (pengecatan, pemberian minyak, electroplating, dan lain-lain), dan perlindungan katodik. Perlindungan katodik dilakukan dengan cara menghubungkan logam yang akan dilindungi dengan logam lain yang mempunyai potensial elektrode yang sangat rendah (biasanya Mg).
Berikut ini analisis untuk masing-masing percobaan:
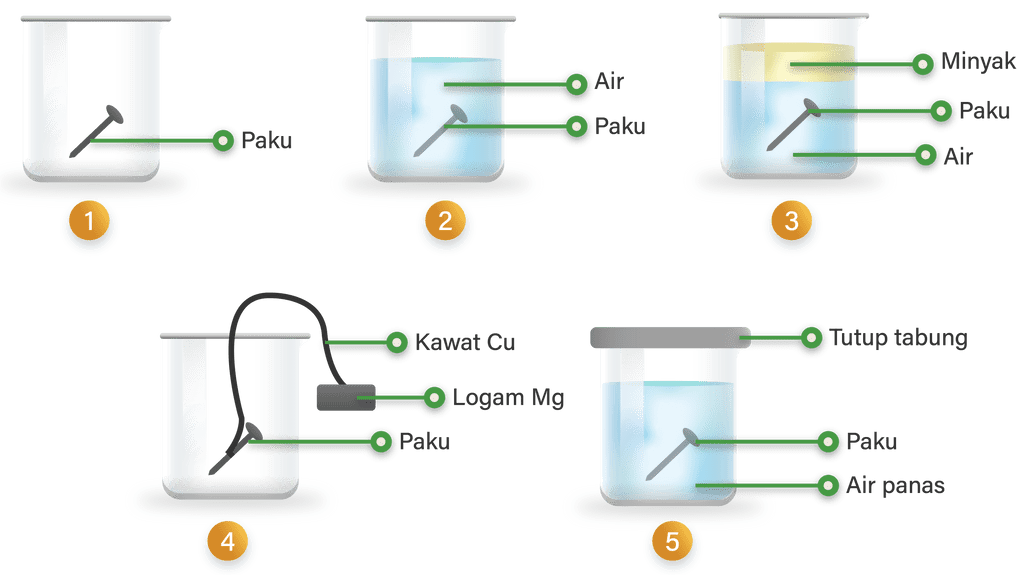
Percobaan 1: Paku diletakkan pada wadah terbuka tanpa air. Korosi dapat berlangsung pada paku ini namun akan berjalan lambat karena hanya mengandalkan oksigen dan air yang ada di udara.
Percobaan 2: Paku diletakkan pada wadah terbuka dengan air. Korosi akan berlangsung cepat karena adanya air dan oksigen.
Percobaan 3: Paku diletakkan pada wadah terbuka dengan air dan minyak. Korosi dapat terjadi karena adanya air. Adanya minyak menghambat oksigen untuk masuk ke dalam air. Korosi pada tabung ini akan lebih lambat dari percobaan kedua.
Percobaan 4: Paku diletakkan pada wadah terbuka dengan dililit tembaga yang terhubung pada logam Mg. Pada deret volta E0 Mg<E0 Fe<E0 Cu, sehingga urutan perkaratan yang terjadi adalah logam Mg, kemudian paku besi, dan yang terakhir kawat tembaga. Korosi pada tabung ini akan lebih lambat dari percobaan pertama.
Percobaan 5: Paku diletakkan pada wadah tertutup dengan air panas. Wadah tertutup mencegah oksigen untuk masuk ke dalam wadah. Air panas dapat mempercepat terjadinya korosi karena temperatur tinggi mempercepat laju reaksi. Air panas dalam wadah tertutup juga menyebabkan adanya uap air dalam tabung. Korosi juga dapat terjadi pada tabung ini.
Jadi, perkaratan akan terjadi paling lambat pada percobaan 4.