Iklan
Pertanyaan
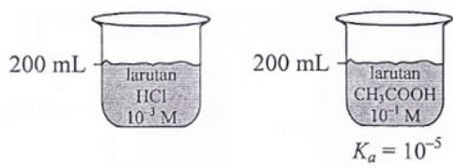
Perhatikan gambar dua larutan berikut ini! Pasangan penjelasan yang tepat mengenai kedua larutan tersebut adalah.... Pernyataan terkait kedua larutan tersebut, antara lain: Kedua larutan sama-sama memiliki pH = 3. Kedua larutan adalah asam lemah. Kedua larutan memiliki harga [ H + ] yang sama. Kedua larutan dapat mengubah warna lakmus merah. Kedua larutan dapat terionisasi sempurna.
Perhatikan gambar dua larutan berikut ini!
Pasangan penjelasan yang tepat mengenai kedua larutan tersebut adalah....
Pernyataan terkait kedua larutan tersebut, antara lain:
- Kedua larutan sama-sama memiliki pH = 3.
- Kedua larutan adalah asam lemah.
- Kedua larutan memiliki harga yang sama.
- Kedua larutan dapat mengubah warna lakmus merah.
- Kedua larutan dapat terionisasi sempurna.
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
7
4.8 (24 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia