Iklan
Pertanyaan
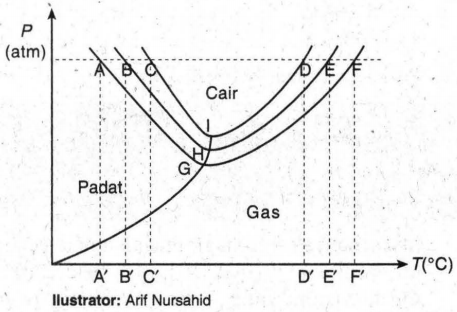
Perhatikan diagram P-T air, larutan KI 0,1 m danlarutan CO(NH 2 ) 2 0,1 m berikut! Kenaikan titik didih larutan KI 0,1 m dan larutanCO(NH 2 ) 2 0,1 mberturut-turut ditunjukkan olehgaris ....
Perhatikan diagram P-T air, larutan KI 0,1 m dan larutan CO(NH2)2 0,1 m berikut!
Kenaikan titik didih larutan KI 0,1 m dan larutan CO(NH2)2 0,1 m berturut-turut ditunjukkan oleh garis ....
IC dan HB
CB dan CA
ID dan DE
DF dan DE
GF dan HE
Iklan
SL
S. Lubis
Master Teacher
Mahasiswa/Alumni Universitas Sumatera Utara
Jawaban terverifikasi
45
5.0 (1 rating)
MC
Melodia Citra
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia