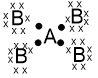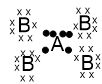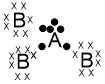Unsur-unsur selain gas mulia dalam mencapai kestabilannya dengan cara melepas atau menangkap elektron supaya memiliki konfigurasi elektron seperti unsur gas mulia.
Pada ikatan kovalen, unsur-unsur yang berikatan berasal dari unsur non logam dimana unsur-unsur tersebut sama-sama membutuhkan elektron dalam mencapai kestabilannya. Oleh karena itu, unsur-unsur tersebut menggunakan pasangan elektron secara bersama. Sedangkan ikatan ion terdiri dari unsur logam dan non logam dimana ikatan ini terjadi serah terima elektron.
Analisis jawaban:
- Jawaban A salah. Ini dikarenakan sebagai berikut:
Atom A memiliki nomor atom 5 sehingga elektron valensinya adalah 3.
Atom B memiliki nomor atom 15 sehingga elektron valensinya adalah 5.
Atom A dalam memenuhi aturan oktet dengan cara melepas 3 elektron sedangkan B dengan cara menangkap 3 elektron sehingga ikatan yang terbentuk adalah ikatan ion dimana atom A akan membentuk ion A3+ dan atom B membentuk ion B3− . Supaya senyawa yang terbentuk bersifat netral, 1 atom A berikatan dengan 1 atom B sehingga rumus moleul yang terbentuk adalah AB.
- Jawaban B salah. Ini dikarenakan sebagai berikut:
Atom A memiliki nomor atom 13 sehingga elektron valensinya adalah 3.
Atom B memiliki nomor atom 35 sehingga elektron valensinya adalah 7.
Atom A dalam memenuhi aturan oktet dengan cara melepaskan 3 elektron sedangkan atom B dengan cara menangkap 1 elektron. Kedua atom tersebut saling melepas dan menangkap elektron sehingga ikatan yang terbentuk adalah ikatan ion. Atom A akan membentuk ion A3+ dan atom B membentuk ion B−. Supaya senyawa yang terbentuk bersifat netral 1 atom A berikatan dengan 3 atom B sehingga rumus molekul yang terbentuka adalah AB3. Senyawa AB3 tidak memiliki PEI dan PEB karena ikatan yang terbentuk adalah ikatan ion.
- Jawaban C salah. Ini dikarenakan sebagai berikut:
Atom A memiliki nomor atom 14 sehingga elektron valensinya adalah 4.
Atom B memiliki nomor atom 35 sehingga elektron valensinya adalah 7.
Atom A dalam memenuhi aturan oktet dengan menangkap 4 elektron sedangkan atom B dengan menangkap 1 elektron. Kedua atom tersebut sama-sama membutuhkan elektron sehingga ikatan yang terbentuk adalah ikatan kovalen. Untuk membentuk senyawa yang memenuhi aturan oktet, 1 atom A berikatan dengan 4 atom B sehingga rumus molekulnya adalah AB4. Struktur Lewis dari AB4 sebagai berikut:
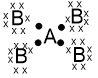
Berdasarkan struktur Lewis, AB4 memiliki 4 PEI dan tidak memiliki PEB.
- Jawaban D benar. Ini dikarenakan sebagai berikut:
Atom A memiliki nomor atom 16 sehingga elektron valensinya adalah 6.
Atom B memiliki nomor atom 35 sehingga elektron valensinya adalah 7.
Atom A dalam memenuhi aturan oktet dengan menangkap 2 elektron sedangkan atom B dengan menangkap 1 elektron. Kedua atom tersebut sama-sama membutuhkan elektron sehingga ikatan yang terbentuk adalah ikatan kovalen. Struktur Lewis dari AB4 sebagai berikut:
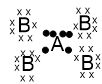
Berdasarkan struktur Lewis, AB4 memiliki 4 dan 1 PEB.
- Jawaban E salah. Ini dikarenakan sebagai berikut:
Atom A memiliki nomor atom 34 sehingga elektron valensinya adalah 6.
Atom B memiliki nomor atom 17 sehingga elektron valensinya adalah 7.
Atom A dalam memenuhi aturan oktet dengan menangkap 2 elektron sedangkan atom B dengan menangkap 1 elektron. Kedua atom tersebut sama-sama membutuhkan elektron sehingga ikatan yang terbentuk adalah ikatan kovalen. Struktur Lewis dari AB3 sebagai berikut:
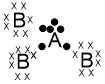
Berdasarkan struktur Lewis, AB3 memiliki 3 PEI dan 3 elektron yang tidak berikatan.
Jadi, jawaban yang benar adalah D.