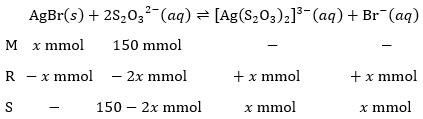Iklan
Pertanyaan
Padatan AgBr (massa molekul 188) dimanfaatkan di bidang fotografi dengan dilarutkan ke dalam larutan Na 2 S 2 O 3 .Ion Ag + dengan ion S 2 O 3 2 − membentuk ion kompleks dengan persamaan reaksi sebagai berikut. AgBr ( s ) ⇌ Ag + ( a q ) + Br − ( a q ) K sp = 5 , 4 × 1 0 − 13 Ag + ( a q ) + 2 S 2 O 3 2 − ( a q ) ⇌ [ Ag ( S 2 O 3 ) 2 ] 3 − ( a q ) K f = 2 , 0 × 1 0 13 Padatan AgBr yang dapat larut dalam 125 mL larutan 1,20 M sebanyak ....
Padatan AgBr (massa molekul 188) dimanfaatkan di bidang fotografi dengan dilarutkan ke dalam larutan . Ion dengan ion membentuk ion kompleks dengan persamaan reaksi sebagai berikut.
Padatan AgBr yang dapat larut dalam 125 mL larutan 1,20 M sebanyak ....
7,14 g
12,24 g
14,08 g
16,72 g
65,10 g
Iklan
SI
S. Ibabas
Master Teacher
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia