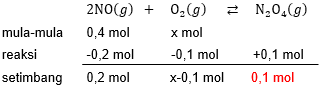Iklan
Pertanyaan
Pada suhu tertentu, harga tetapan kesetimbangan untuk reaksi: 2 NO ( g ) + O 2 ( g ) ⇄ N 2 O 4 ( g ) adalah 12,5. Dalam ruang 1 liter, 0,4 mol NO direaksikan dengan gas O 2 . Jika pada saat setimbang ditandai dengan terbentuknya N 2 O 4 sebanyak 0,1 mol, maka besarnya mol gas mula-mula adalah ....
Pada suhu tertentu, harga tetapan kesetimbangan untuk reaksi:
adalah 12,5. Dalam ruang 1 liter, 0,4 mol NO direaksikan dengan gas . Jika pada saat setimbang ditandai dengan terbentuknya sebanyak 0,1 mol, maka besarnya mol gas mula-mula adalah ....
1
0,5
0,3
0,1
0,05
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
24
5.0 (4 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia