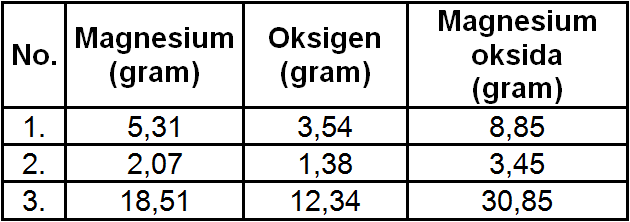
Berdasarkan data di atas, hukum Proust berlaku pada reaksi antara magnesium dengan oksigen membentuk magnesium oksida. Hal ini disebabkan massa magnesium dan oksigen dalam setiap percobaan memiliki pebandingan yang sama dan tetap, yaitu 3 : 2.
Pada tahun 1799, Joseph Louis Proust menemukan satu sifat penting dari senyawa, yang disebut Hukum Perbandingan Tetap. Berdasarkan penelitian terhadap berbagai senyawa yang dilakukannya, Proust menyimpulkan bahwa: “Perbandingan massa unsur-unsur dalam satu senyawa adalah tertentu dan tetap.“
Tabel pada soal di atas menunjukkan data massa pereaksi (magnesium dan oksigen) dan produk (magensium oksida) dalam 3 buah percobaan. Untuk dapat mengetahui apakah data percobaan tersebut sesuai dengan hukum Proust, maka perlu dihitung perbandingan massa Mg : massa O pada setiap percobaan. Perhitungan perbandingan massa Mg : massa O pada tiap percobaan adalah sebagai berikut.
- Percobaan ke-1.
massa Mg : massa Omassa Mg : massa Omassa Mg : massa Omassa Mg : massa O====5,31 g : 3,54 g3,545,31:3,543,541,5 : 13 : 2
- Percobaan ke-2.
massa Mg : massa Omassa Mg : massa Omassa Mg : massa Omassa Mg : massa O====2,07 g : 1,38 g1,382,07:1,381,381,5 : 13 : 2
- Percobaan ke-3.
massa Mg : massa Omassa Mg : massa Omassa Mg : massa Omassa Mg : massa O====18,51 g : 12,34 g12,3418,51:12,3412,341,5 : 13 : 2
Berdasarkan perhitungan tersebut, diketahui bahwa perbandingan massa Mg : massa O = 3 : 2, dan perbandingan ini konstan atau tetap nilainya pada semua percobaan.
Dengan demikian, maka pada reaksi antara magnesium dengan oksigen membentuk magnesium oksida tersebut berlaku hukum Proust karena perbandingan massa Mg dan massa O nilainya selalu konstan di setiap percobaan yaitu 3 : 2.