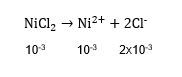Iklan
Pertanyaan
Pada 25 ∘ C , Ksp Ni ( OH ) 2 = 6 × 1 0 − 18 . Hitunglah, kelarutan Ni ( OH ) 2 dalam: c. Larutan NiCl 2 0,001 M
Pada , Ksp . Hitunglah, kelarutan dalam:
c. Larutan 0,001 M
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
5
4.0 (1 rating)
SK
Syarifah Khairani manik
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia