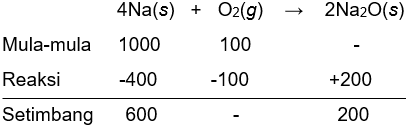Iklan
Pertanyaan
Natrium bereaksi dengan oksigenmembentuk natrium oksida menurut reaksiberikut. 4 Na ( s ) + O 2 ( g ) → 2 Na 2 O ( s ) Apabila 1.000 atom natrium direaksikandengan 100 molekul oksigen, jumlahmolekul Na 2 O sebanyak-banyaknya yangdapat terbentuk adalah ...
Natrium bereaksi dengan oksigen membentuk natrium oksida menurut reaksi berikut.
Apabila 1.000 atom natrium direaksikan dengan 100 molekul oksigen, jumlah molekul sebanyak-banyaknya yang dapat terbentuk adalah ...
100
200
500
1.000
1.100
Iklan
AC
A. Chandra
Master Teacher
Mahasiswa/Alumni Universitas Negeri Jakarta
Jawaban terverifikasi
6
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia