Menurut aturan Hund, setiap orbital harus berisi 1 elektron dengan arah (spin) yang sama. Elektron selanjutnya yang mengisi orbital harus memiliki arah (spin) yang berbeda. Pengisian elektron juga harus mengikuti prinsip Aufbau yaitu pengisiannya dimulai dari orbital yang memiliki tingkat energi terendah ke tingkat energi yang lebih tinggi.
Pada pilihan jawaban dapat diidentifikasi bahwa.
A. 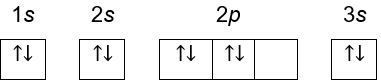
Tidak memenuhi aturan Hund, karena pada subkulit atom 2p belum terisi penuh di kotak ketiga, namun sudah mengisi spin bawah di kotak pertama dan kotak kedua.
B. 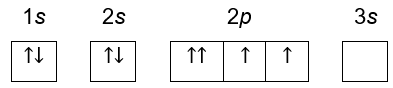
Tidak memenuhi larangan pauli, pada subkulit 2p memiliki dua spin dengan arah yang sama.
C. 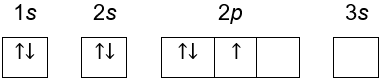
Tidak memenuhi aturan hund karena subkulit 2p belum terisi penuh di kotak ketiga, namun sudah mengisi spin bawah di kotak pertama.
D. 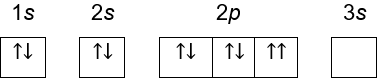
Tidak memenuhi larangan pauli, pada subkulit 2p memiliki dua spin dengan arah yang sama.
E. 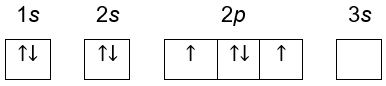
Tidak memenuhi karena penulisan spin bawah yang terletak pada 2p kotak kedua. Seharunsya berada pada kotak pertama. Hal ini akan berdampak apabila kita hendak menentukan bilangan kuantum magnetiknya.
Dari penjelasan tersebut, tidak ada yang mengikuti aturan Hund.
Jadi, tidak ada pilihan jawaban yang benar.