Semua atom dapat diidentifikasi berdasarkan jumlah proton dan neutron yang dikandungnya. Jumlah proton dalam inti setiap atom suatu unsur disebut nomor atom (atomic number). Nomor atom diberi lambang Z. Nomor atom suatu unsur merupakan ciri khas atom unsur tersebut. Muatan atom suatu unsur selalu netral. Oleh karena itu, jumlah proton sama dengan jumlah elektron. Hubungan antara nomor atom, proton, dan elektron dapat dituliskan sebagai berikut.
Nomor atom = Z = jumlah proton = jumlah elektron
Nomor massa (mass number) adalah jumlah neutron dan proton yang ada dalam inti atom suatu unsur. Nomor massa diberi lambang A. Massa elektron sangat kecil dibandingkan massa proton dan neutron sehingga dapat diabaikan. Secara umum, hubungan antara nomor massa, proton, dan neutron dapat dituliskan sebagai berikut.
Nomor massa =A = jumlah proton + jumlah neutron
Secara umum notasi atom bisa dituliskan seperti berikut:
ZAUnsur
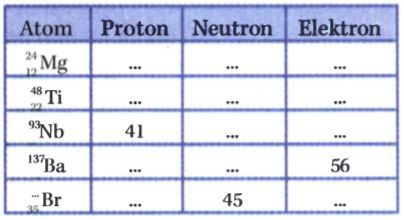
Untuk melengkapi tabel yang rumpang tersebut maka,
- Jumlah proton Mg = jumlah elektron Mg = Nomor atom = 12
- Jumlah neutron Mg = nomor massa-nomor atom = 24-12 = 12
- Jumlah proton Ti = jumlah elektron = nomor atom = 22
- Jumlah neutron Ti = nomor massa-nomor atom = 48-22 = 26
- Jumlah proton Nb = jumlah elektron = nomor atom = 41
- Jumlah neutron Nb = nomor massa-nomor atom = 93-41 = 52
- Jumlah proton Ba = jumlah elektron = nomor atom = 56
- Jumlah neutron Ba = nomor massa-nomor atom = 137-56 = 81
- Jumlah proton Br = jumlah elektron = nomor atom = 35
- Jumlah neutron Br = nomor massa-nomor atom = 45
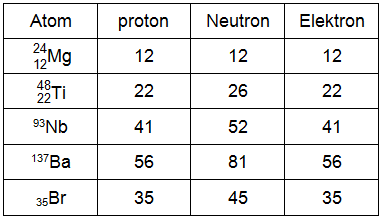
Jadi, tabel yang telah dilengkapi adalah seperti berikut.