Iklan
Pertanyaan
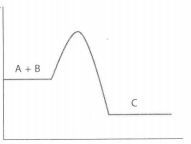
Kurva tingkat energi dan jalannya reaksi dari reaksi: A + B → C : Dari kurva tersebut dapat dinyatakan bahwa ....
Kurva tingkat energi dan jalannya reaksi dari reaksi: :
Dari kurva tersebut dapat dinyatakan bahwa ....
Reaksi:
merupakan reaksi eksoterm.
Reaksi:
merupakan endoterm.
Reaksi tersebut tidak memerlukan katalis.
Energi aktivasinya lebih tinggi daripada nilai perubahan entalpinya.
Reaksinya mudah berlangsung pada suhu rendah.
Iklan
SL
S. Lubis
Master Teacher
Mahasiswa/Alumni Universitas Sumatera Utara
Jawaban terverifikasi
1
4.8 (6 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia