Iklan
Pertanyaan
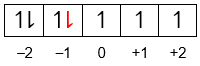
Kobalt adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Co dan nomor atom 27. Elemen ini biasanya hanya ditemukan dalam bentuk campuran di alam. Bilangan kuantum elektron terakhir atom tersebut adalah ....
Kobalt adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Co dan nomor atom 27. Elemen ini biasanya hanya ditemukan dalam bentuk campuran di alam. Bilangan kuantum elektron terakhir atom tersebut adalah ....
Iklan
MB
M. Banyu
Master Teacher
Jawaban terverifikasi
3
5.0 (1 rating)
MO
Marco Ones Y Jaya
Pembahasan lengkap banget Mudah dimengerti Makasih ❤️ Bantu banget Ini yang aku cari!
Iklan
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia