Iklan
Pertanyaan
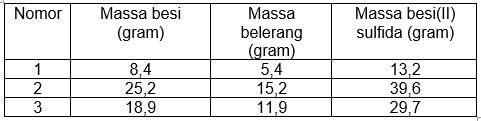
Jika unsur besi direaksikan dengan unsur belerang akan menghasilkan senyawa besi(II) sulfida. Data percobaan terdapat pada tabel berikut. Diketahui selama percobaan digunakan belerang berlebih. Perbandingan massa besi terhadap belerang adalah ....
Jika unsur besi direaksikan dengan unsur belerang akan menghasilkan senyawa besi(II) sulfida. Data percobaan terdapat pada tabel berikut.
Diketahui selama percobaan digunakan belerang berlebih. Perbandingan massa besi terhadap belerang adalah ....
5 : 6
6 : 5
4 : 5
5 : 4
7 : 4
Iklan
JS
J. Siregar
Master Teacher
Mahasiswa/Alumni Universitas Negeri Medan
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia