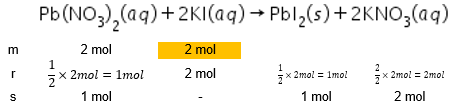Iklan
Pertanyaan
Jika larutan yang mengandung 2 mol Pb ( NO 3 ) 2 direaksikan dengan larutan yang mengandung 2 mol KI sesuai reaksi: Pb ( NO 3 ) 2 ( a q ) + 2 KI ( a q ) → PbI 2 ( s ) + 2 KNO 3 ( a q ) maka akan dihasilkan PbI 2 sebanyak ... .
Jika larutan yang mengandung 2 mol direaksikan dengan larutan yang mengandung 2 mol sesuai reaksi:
maka akan dihasilkan sebanyak ... .
4 mol
2 mol
1 mol
0,5 mol
0,2 mol
Iklan
IY
I. Yassa
Master Teacher
Jawaban terverifikasi
4
4.7 (59 rating)
Ni
Naomi ivana Uli sagala
Pembahasan lengkap banget
PS
Putri Supina putri
Ini yang aku cari!
M
M.Zaidan
Mudah dimengerti
i
indah
Pembahasan terpotong Jawaban tidak sesuai
oA
olivia Amanda
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia