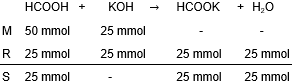Iklan
Pertanyaan
Jika 1,4gram KOH ( Mr = 56 g mol − 1 ) dimasukkan ke dalam 500 mLHCOOH 0,1 M ( K a = 1 0 − 5 ) , akan menghasilkan larutan penyangga ... dengan pH ...
Jika 1,4 gram KOH dimasukkan ke dalam 500 mL HCOOH 0,1 M , akan menghasilkan larutan penyangga ... dengan pH ...
Iklan
IN
I. Nur
Master Teacher
Mahasiswa/Alumni Universitas Negeri Malang
Jawaban terverifikasi
2
4.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia