Iklan
Pertanyaan
Iodin (I) dan fluorin (F) membentuk deret senyawa biner dengan komposisi sebagai berikut. a. Hitunglah massa fluorin yang bergabung dengan 1 g iodin untuk setiap data tersebut! b. Dengan membuat nisbah bilangan bulat terkecil di antara keempat jawaban pada (a), tunjukkan bahwa senyawa-senyawa tersebut memenuhi Hukum Perbandingan Berganda!
Iodin (I) dan fluorin (F) membentuk deret senyawa biner dengan komposisi sebagai berikut.
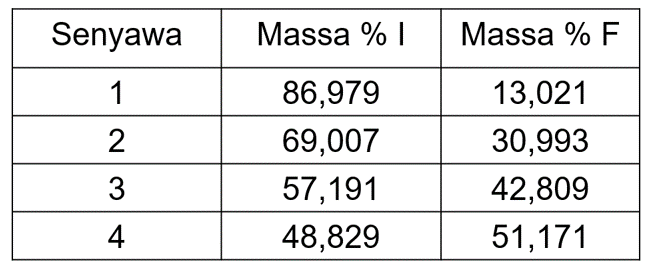
a. Hitunglah massa fluorin yang bergabung dengan 1 g iodin untuk setiap data tersebut!
b. Dengan membuat nisbah bilangan bulat terkecil di antara keempat jawaban pada (a), tunjukkan bahwa senyawa-senyawa tersebut memenuhi Hukum Perbandingan Berganda!
Iklan
C. Rhamandica
Master Teacher
Mahasiswa/Alumni Universitas Negeri Malang
11
4.0 (1 rating)
Sevni Sevni
Ini yang aku cari!
Iklan
Pertanyaan serupa
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia