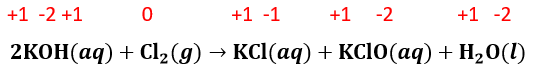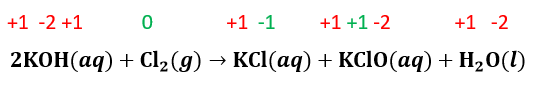Iklan
Pertanyaan
Hubungan yang tepat antara atom dan perubahan bilangan oksidasi menurut reaksi: 2 KOH ( a q ) + Cl 2 ( g ) → KCl ( a q ) + KClO ( a q ) + H 2 O ( l ) adalah ....
Hubungan yang tepat antara atom dan perubahan bilangan oksidasi menurut reaksi:
adalah ....
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
1
4.8 (36 rating)
Na
Nurul azizah Muhammad
Mudah dimengerti Makasih ❤️ Bantu banget
Sa
Siyam argiani Holijah
Makasih ❤️
S
Syaripah
Makasih ❤️
HN
Hanum Nabilla
Pembahasan lengkap banget
RN
Revalina Nesya Aulia
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia